Офлоксацин: почему мы выбираем именно его? Левофлоксацин: аналоги по действующему веществу, особенности терапевтического эффекта и показания к приему Что лучше левофлоксацин или ципрофлоксацин.
Офлоксацин относится к фторхинолонам І поколения - высокоактивным антибактериальным препаратам, прочно вошедшим в медицинскую практику. Препараты этой группы можно рассматривать как альтернативу антибиотикам широкого спектра действия. Следует отметить, что лекарственные средства этой группы отличаются по фармакокинетическим свойствам и специфической антибактериальной активности. К группе фторхинолонов относятся офлоксацин и ципрофлоксацин (выпускаются в форме таблеток и раствора для инъекций).
Благодаря своей структуре и механизму действия офлоксацин обладает высокой бактерицидной активностью, сопоставимой с таковой цефалоспоринов ІІІ поколения. Препарат активен в отношении грамотрицательных и грамположительных микроорганизмов, включая штаммы, резистентные к другим антибактериальным препаратам, а также штаммы атипичных внутриклеточных возбудителей.
Офлоксацин обладает оптимальным фармакокинетическим профилем, хорошо всасывается в пищеварительном тракте (около 100%), за счет быстрого проникновения в ткани в месте инфекции создается высокая концентрация препарата, период полувыведения составляет 5–7 ч.
Офлоксацин можно назначать одновременно со многими антибактериальными препаратами (макролидами, b -лактамными антибиотиками, цефалоспоринами). Благодаря этому свойству препарат широко используют в составе комбинированной терапии при инфекционных заболеваниях. Офлоксацин, в отличие от ципрофлоксацина, сохраняет активность при одновременном применении ингибиторов синтеза РНК-полимеразы (хлорамфеникола и рифампицина).
По химическому строению многие фторхинолоны, в том числе содержащие больше одного атома фтора, относятся к бициклическим производным. Как показали результаты многочисленных исследований (Падейская Е.Н., 1994, 1996), дополнительное фторирование не изменяет спектр и выраженность антибактериальной активности. Физико-химические свойства, обусловливающие особенности фармакокинетики и противомикробной активности препаратов этой группы, в большей степени зависят от их строения - бицикличности или трицикличности.
Офлоксацин относится к группе трициклических монофторхинолонов. В отличие от ципрофлоксацина он практически не метаболизируется в печени. Биодоступность офлоксацина при пероральном приеме и парентеральном введении идентична. Благодаря этому при замене инъекционного способа введения препарата пероральным коррекции дозы не требуется (одно из существенных отличий офлоксацина от ципрофлоксацина).
Согласно рекомендациям ВОЗ, 200 мг офлоксацина соответствуют 500 мг ципрофлоксацина.
Он хорошо проникает в органы-мишени (например, при хроническом простатите - в ткань предстательной железы). Следует отметить, что при простатите капсула предстательной железы практически не проницаема для многих антибактериальных препаратов.
Между используемой дозой офлоксацина и его концентрацией в тканях существует линейная зависимость.
Офлоксацин назначают 1–2 раза в сутки. Прием пищи не влияет на его всасываемость, однако при употреблении жирной пищи всасывание офлоксацина замедляется.
Офлоксацин в меньшей степени, чем ципрофлоксацин, взаимодействует с другими препаратами, практически не влияет на кинетику теофиллина и кофеин-бензоата натрия.
Офлоксацин выделяется преимущественно почками (более 80%) в неизмененном виде, то есть этот препарат не обладает эффектом первичного прохождения через печень. Концентрация офлоксацина в кале значительно ниже, чем ципрофлоксацина. Однако этот препарат более эффективен при диарее бактериального генеза, а также при диарее путешественников. Это обусловлено его более выраженной активностью в отношении стафилококков и сальмонелл. Противомикробная активность офлоксацина в наибольшей степени выражена в отношении грамотрицательных бактерий и внутриклеточных патогенов (хламидий, микоплазм, уреаплазм), в отношении стрептококков и синегнойной палочки офлоксацин менее активен.
Бактерицидная эффективность офлоксацина проявляется достаточно быстро, резистентность микроорганизмов к этому препарату развивается редко. Это обусловлено его бактерицидным механизмом действия, влияющим только на один ген ДНК-гиразы и на топоизомеразу.
В клинической практике офлоксацин является препаратом выбора или альтернативным препаратом первого ряда, его рекомендуют для эмпирической терапии при многих урогенитальных инфекциях. Благодаря хорошей переносимости (частота развития побочных эффектов - 1,3%), высокой биодоступности препарата в форме таблеток и оптимальному спектру действия (активен в отношении 94% патогенов, вызывающих инфекции урогенитального тракта, кроме простейших и анаэробов) его можно использовать в амбулаторных условиях. Существенным преимуществом офлоксацина при лечении инфекций мочевых путей является его высокая концентрация как в паренхиме почек, так и в чашечно-лоханочном аппарате. Результаты клинических исследований (Падейская Е.Н., Яковлев В.П., 1995; Lynne C., 1996) свидетельствуют о том, что офлоксацин при сравнении его с другими антибиотиками оказывает более выраженное антибактериальное действие в отношении хламидий, и его эффективность сопоставима с другими фторхинолонами и доксициклином в отношении микоплазм и уреаплазм.
При остром цистите офлоксацин является препаратом выбора. Это заболевание чаще диагностируют у женщин (0,5–0,7 эпизодов в год на 1 женщину).
При хроническом цистите у лиц молодого возраста, особенно при наличии сопутствующих инфекций, передающихся половым путем (20–40% случаев, вызванных хламидиями, микоплазмами и уреаплазмами), офлоксацин является приоритетным среди других фторхинолонов.
Частота выявления хламидий у больных гинекологического профиля составляет 40%. В основном это женщины молодого возраста с бесплодием, воспалительными заболеваниями органов малого таза, пациентки с указанием в анамнезе на внематочную беременность. У 70% больных хламидиоз сочетается с инфицированием другими микроорганизмами, что усугубляет течение воспалительного процесса и требует назначения адекватной терапии (сочетание с уреаплазмой выявляют в 33% случаев, с микоплазмой - в 21%, гарднереллой - приблизительно в 14%, грибами рода Candida - в 12,9%. Офлоксацин эффективен в отношении всех перечисленных возбудителей, кроме грибов рода Candida .
Офлоксацин - единственный фторхинолон, рекомендуемый Ассоциацией урогенитальной медицины и Медицинским обществом изучения венерических заболеваний (США) в качестве альтернативного препарата первого выбора для лечения больных с негонококковым уретритом и хламидийной инфекцией урогенитального тракта (1999). Центр по контролю и профилактике заболеваний (США, 1993) рекомендует применять офлоксацин в комбинации с метронидазолом или клиндамицином для лечения пациенток с воспалительными заболеваниями органов малого таза в амбулаторных условиях.
На украинском фармацевтическом рынке представлен новый препарат группы фторхинолонов производства компании «Лечива» (Чехия). ОФЛОКСИН 200, который зарегистрирован в нашей стране в форме таблеток по 200 мг (10 таблеток в упаковке). Оценивая качество ОФЛОКСИНА 200, хотелось бы отметить, что по биоэквивалентности он полностью соответствует оригинальному стандарту и требованиям GMP. Это значит, что больные реже будут повторно обращаться к врачу по поводу рецидивов заболевания и развития побочных эффектов. Предлагая пациенту ОФЛОКСИН 200, вы можете быть уверены, что выбор сделан правильно.
Н.А. Горчакова, проф., д-р мед. наук
Национальный медицинский университет им. А.А. Богомольца
Большой популярностью в лечении инфекционно-воспалительных заболеваний пользуются фторхинолоны. Часто врачи назначают Левофлоксацин или Ципрофлоксацин, сравнение этих препаратов поможет определить, в каких случаях тот или иной медикамент окажет положительное действие.
Характеристика Левофлоксацина
Левофлоксацин — синтетически созданный антибиотик-фторхинолон. В качестве действующего вещества препарата выступает изомерный аналог офлоксацина. Одна таблетка содержит 250 мг левофлоксацина гемигидрата.
Показаниями к применению являются инфекционные болезни, вызываемые чувствительной микрофлорой:
- острые синуситы;
- хронический бронхит в острой стадии;
- воспаление легких;
- инфекции мочевыделительного тракта;
- простатиты;
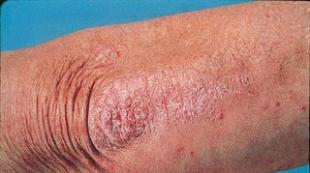
- инфекционные поражения кожи;
- инфекции желудочно-кишечного тракта.
Средняя суточная доза при пероральном приеме составляет 500 мг.
Не назначается, если у пациента наблюдаются аллергические реакции на один из компонентов, входящих в состав препарата.
Также противопоказан при таких клинических картинах:
- эпилепсия;
- проблемы с сухожилиями при применении фторхинолов.
Не используют лекарственное средство в педиатрии (возможно нарушение суставного хряща).
Не проводят лечение медикаментами в период беременности и грудного вскармливания.
В редких случаях могут наблюдаться следующие отрицательные последствия:
- кандидоз;
- микозы;
- воспаление и дистрофия ткани сухожилия, разрывы;
- снижение количества лейкоцитов, тромбоцитов или эритроцитов;
- анафилактический шок;
- анорексия, гипогликемия;
- нарушение сна, нервозность, раздражительность;
- расстройство вкуса;
- тремор конечностей;
- вертиго, звон в ушах;
- тахикардия, артериальная гипотензия, удлинения интервала QT;
- бронхоспазм, нехватка воздуха, аллергический пневмонит;
- тошнота, рвота, диспепсия, диарея;
- гепатит, желтуха;
- сыпь, зуд, ангионевротический отек, гипергидроз;
- нарушение почечных функций;
- астения, пирексия, боль в груди, спине, конечностях;
- приступы порфирии.

При употреблении препарата в больших дозах, чем рекомендовано, могут появиться такие симптомы:
- головокружение, потеря сознания;
- судороги;
- удлинение QT-интервала.
При передозировке нужно сразу прекратить прием медикамента, обратиться к врачу, сделать ЭКГ.
Диализ неэффективен, потому что антидот отсутствует. Лечение может быть только симптоматическим.
Характеристика Ципрофлоксацина
Основное действующее вещество препарата — ципрофлаксацин. В состав медикамента входят вспомогательные компоненты: крахмал, тальк, диоксиды титана и кремния, стеарат магния и лецитин.
Показаниями к применению лекарственного препарата являются:
- острый бронхит, обострения заболевания в хронической форме;
- тяжелая форма туберкулеза;
- легочное воспаление;
- инфекции, развивающиеся вследствие муковисцидоза;
- воспаление среднего уха — отит;
- гаймориты;
- фронтит;
- фарингит;
- тонзиллит;
- усложненные инфекции и воспаления мочевой системы;
- хламидиоз;
- гонорея;
- инфекционные заболевания ЖКТ;
- инфекционные кожные повреждения, ожоги, язвы и ряд других.
Лекарственное средство может применяться при лечении послеоперационных инфекционных осложнений.
Нельзя принимать Ципрофлоксацин при аллергических реакциях на главное и вспомогательные составляющие медикамента, a также одновременном применении тизанидина.
Противопоказано применять беременным женщинам и кормящим грудью.
Побочные эффекты:
- жидкий стул;
- рвотные позывы;
- эозинофилия;
- грибковые суперинфекции;
- отсутствие аппетита;
- возбуждение;
- гиперактивность;
- головные боли;
- нарушения вкуса;
- головокружение;
- расстройства сна;
- метеоризм;
- боли в области желудка/кишечника;
- повышенная активность ферментов печени;
- костно-мышечные боли;
- суставные боли;
- сыпь, крапивная лихорадка;
- повышение температуры, усталость;
- изменение количества лейкоцитов;
- воспаление ободочной кишки;
- снижение количества тромбоцитов;
- повышение уровня сахара;
- аллергические реакции;
- депрессия c появлением суицидальных мыслей;
- патологические сновидения;
- изменения чувствительности;
- дрожание;
- судороги;
- нарушение зрения;
- снижение артериального давления;
- тахикардия;
- обморок;
- нарушения работы печени;
- удушье;
- желтуха, гепатит;
- непереносимость солнечного света (фоточувствительность);
- повышенный мышечный тонус.

При превышении дозы лекарства нужно прекратить прием и обратиться за медицинской помощью.
Симптомы передозировки могут быть следующими:
- головная боль;
- усталость;
- спутанность сознания;
- головокружения;
- судороги;
- галлюцинации;
- чувство дискомфорта в животе;
- появление кристаллов, крови в моче;
- нарушение работы почек/печени.
Сравнение препаратов
Ципрофлоксацин и Левофлоксацин — медикаменты-аналоги. Они применяются в области пульмонологии и отоларингологии. Их используют в терапии болезней, связанных с воспалением ЛОР-органов, респираторные инфекции тоже не являются исключением. При этом в состав препаратов входят разные действующие вещества, поэтому между лекарственными средствами есть различия.
Сходство
Оба медикамента принадлежат к антибиотикам из ряда фторхинолонов. Левофлоксацин и Ципрофлоксацин имеют схожее предназначение, поэтому и спектр действий их идентичен.
Лекарственные средства имеют одинаковые формы выпуска:
- таблетки;
- раствор (для инъекций и для инфузий);
- капли (глазные и ушные).
Препараты хорошо переносятся организмом и хорошо всасываются при употреблении внутрь. Побочные реакции возникают редко и с одинаковой периодичностью. Отрицательные последствия тоже схожи.
В чем разница
Действующее вещество Левофлоксацина — левофлоксацин, главный компонент Ципрофлоксацина — офлоксацин. Первый является новым медикаментом, а второй относится к препаратам первого поколения, поэтому часть болезнетворных бактерий выработали устойчивость к нему.
Новый препарат совместим с другими медикаментами, у Ципрофлоксацина при взаимодействии с иными составами уровень активности снижается.
Что дешевле
Любая форма Ципрофлоксацина дешевле, чем оппонента. Например, средняя стоимость упаковки таблеток первого — 80 руб., второго — 250 руб.
Можно ли заменить Левофлоксацин на Ципрофлоксацин
Левофлоксацин можно заменить на Ципрофлоксацин, если бактерии, которые вызвали заболевание, восприимчивы к последнему. Перед тем как произвести замену, лучше проконсультироваться с врачом.
Что лучше — Левофлоксацин или Ципрофлоксацин
Левофлоксацин, являясь препаратом нового поколения, обладает более высокой эффективностью. Некоторые возбудители, которые устойчивы к оппоненту, не могут противостоять Левофлоксацину. Он более активен в отношении Pseudomonas aeruginosa, пневмококковой инфекции и атипичных микроорганизмов.
Огромное количество инфекционно-воспалительных заболеваний, вызванных различными возбудителями, заставляет врачей использовать для борьбы с ними антибактериальные препараты, отличающиеся широким спектром действия. Особой популярностью пользуются фторхинолоны. Доверие врачей и пациентов заслужили Ципрофлоксацин и Левофлоксацин сравнение которых помогает понять, в каких случаях тот или иной препарат позволит добиться положительного результата в самые короткие сроки и без вреда для общего состояния больного.
Ципрофлоксацин входит в число антибактериальных препаратов, обладающих широким спектром активности и применяемый в качестве средства для борьбы с возбудителями воспалительных процессов, поражающих органы:
- Дыхания.
- Мочевой и половой систем.
- Брюшной полости.
Высокой эффективностью Ципрофлоксацин отличается при проведении терапевтических мероприятий, направленных на устранение патологического процесса, возникающего в организме человека и провоцирующего развитие:
- Воспаления бронхов и лёгких.
- Муковисцидоза.
- Бронхоэктатической болезни.
- Фарингита и воспаления гайморовых пазух (гайморита).
- Отита, тонзиллита и синусита.
- Инфекции в почках, мочевыводящих путях, мочевом пузыре и уретре.
- Аднексита и простатита.
- Гонореи и хламидиоза.
- Заболеваний органов желудочно-кишечного тракта (вызванных проникновением болезнетворных бактерий).
- Инфекций дермы и мягких тканей.
- Недугов, поражающих костный каркас и суставной аппарат (остеомиелит, септический артрит).
Несмотря на то что фторхинолоны давно пользуются повышенной популярностью у ЛОР врачей, их применение оправдано при терапии заболеваний, поражающих мочеполовую систему мужчин. Так, при лечении простатита Ципрофлоксацин назначается чаще других антибиотиков и позволяет в самые короткие сроки добиться полного выздоровления пациента.
 Препарат используется в качества средства, уничтожающего болезнетворные микроорганизмы, отличающиеся высокой степенью чувствительности к ципрофлоксацину и бактерии, вырабатывающие бета-лактамазу. Лекарственный препарат «Ципрофлоксацин» обладает бактерицидным действием, угнетает выработку ДНК бактерий и отличается способностью подавлять ДНК-гиразу.
Препарат используется в качества средства, уничтожающего болезнетворные микроорганизмы, отличающиеся высокой степенью чувствительности к ципрофлоксацину и бактерии, вырабатывающие бета-лактамазу. Лекарственный препарат «Ципрофлоксацин» обладает бактерицидным действием, угнетает выработку ДНК бактерий и отличается способностью подавлять ДНК-гиразу.
Активность антибиотика проявляется в отношении:
- Стафило- и стрептококков.
- Шигеллы.
- Сальмонеллы.
- Нейссерий.
- Хламидий.
- Микоплазмы.
- Клостридий.
Ципрофлоксацин быстро всасывается в слизистую ЖКТ (желудочно-кишечного тракта) независимо от приёма пищи. Хорошо распределяется в тканях и клетках человеческого организма.
Несмотря на высокую результативность препарата, существуют противопоказания к его применению и риск возникновения побочных эффектов.
Среди состояний, при которых лечение с помощью Ципрофлоксацина противопоказано:
- Беременность (особенность первый триместр).
- Период грудного вскармливания (лактации).
- Младший детский возраст.
- Индивидуальная непереносимость активного действующего компонента и высокий уровень чувствительности к фторхинолонам.
 Запрещено использовать Ципрофлоксацин в качестве лекарственного средства и в тех случаях, когда пациент не достиг возраста 18 лет.
Запрещено использовать Ципрофлоксацин в качестве лекарственного средства и в тех случаях, когда пациент не достиг возраста 18 лет.
От использования антибиотика следует отказаться при появлении побочных эффектов:
- Тошноты и частых позывов к рвоте.
- Нарушении пищеварения (диспепсии).
- Изменении стула (диареи).
- Сбоя сердечного ритма и учащении сердцебиения (тахикардии).
- Нарушении функциональности мочевыделительной системы.
- Появлении в урине крови.
- Болей в животе.
- Увеличении содержания билирубина.
Следует немедленно сообщить лечащему врачу о возникшей аллергической реакции, которая проявляется в виде кожного зуда и высыпаний. Возможна отмена препарата, если у больного появились жалобы на отсутствие сна и аппетита, возникновение галлюцинаций и повышенной раздражительности. Помимо прочего, возможны и другие формы негативной реакции. Речь идёт о головокружении, обмороках или ухудшении зрения.
Чтобы избежать возможных неприятностей, следует внимательно изучить инструкцию и строго следовать указаниям, полученным от лечащего врача в отношении режима дозирования и графика приёма лекарства.
В первую очередь нужно учесть, что продолжительность терапии с использованием Ципрофлоксацина не должна превышать 10-14 дней. В течение этого времени приём препарата в виде капсул или таблеток осуществляется дважды в день по 250, 500 или 750 мг. Суточная доза для взрослых пациентов составляет 1,5 г.
 Внутривенное введение проводится 2 р/д с интервалом 12 часов. Разовая доза антибиотика не превышает 400 мг. Несмотря на то что разрешено струйное внутривенное введение раствора, врачи в большинстве случаев рекомендуют использовать капельницу, стараясь обеспечить постепенное медленное проникновение в организм активного действующего компонента.
Внутривенное введение проводится 2 р/д с интервалом 12 часов. Разовая доза антибиотика не превышает 400 мг. Несмотря на то что разрешено струйное внутривенное введение раствора, врачи в большинстве случаев рекомендуют использовать капельницу, стараясь обеспечить постепенное медленное проникновение в организм активного действующего компонента.
Используя Ципрофлоксацин в офтальмологии, инстилляции проводят с интервалом 4 часа и закапывают по 2 капли специального раствора в каждый глаз (нижний конъюнктивальный мешок).
Добиваясь быстрого излечения пациентов, врачи всё чаще назначают антибактериальные препараты широкого спектра воздействия на многочисленные болезнетворные микроорганизмы. В числе лекарственных средств, отличающихся повышенной эффективностью, Левофлоксацин, что пользуется заслуженным доверием офтальмологов, терапевтов, урологов.
Его назначают для лечения таких сложных и опасных заболеваний, как:
- Внебольничное воспаление лёгких.
- Хронический бронхит в стадии обострения.
- Острый синусит, вызванный проникновением в организм болезнетворных бактерий.
- Острый пиелонефрит.
- Инфекционные воспалительные заболевания мочевыводящих путей.
- Хронический бактериальный простатит.
- Гнойные поражения мягких тканей и дермы (абсцессы и фурункулёз).
В качестве одного из составляющих комплексной терапии Левофлоксацин используется при проведении лечебных мероприятий, направленных на борьбу с туберкулёзом.
 Противомикробное бактерицидное действие препарата обеспечивает его активный действующий компонент – гемигидрат левофлоксацина. Созданное на его основе лекарственное средство обладает способностью блокировать ДНК гиразу и вызывать значительные морфологические изменения в мембранах и клетках болезнетворных бактерий. Это губительно действует на патогенные микроорганизмы и препятствует их росту и размножению.
Противомикробное бактерицидное действие препарата обеспечивает его активный действующий компонент – гемигидрат левофлоксацина. Созданное на его основе лекарственное средство обладает способностью блокировать ДНК гиразу и вызывать значительные морфологические изменения в мембранах и клетках болезнетворных бактерий. Это губительно действует на патогенные микроорганизмы и препятствует их росту и размножению.
Чувствительность к Левофлоксацину обнаружена у многих бактерий, в том числе у:
- Стрептококков и энтерококков.
- Стафилококков и клебсиелл.
- Морганелл и нейссерий.
- Хламидий и микоплазмы.
- Риккетсий и уреаплазмы.
После приёма внутрь антибиотик быстро всасывается и легко проникает в лёгкие и слизистую бронхов, органы мочеполовой системы. Большая часть состава выводится в течение суток через почки.
Принимают антибактериальный препарат «Левофлоксацин», выпускаемый в таблетированной форме, запивая большим количеством чистой воды, не разжёвывая и не измельчая предварительно. Суточная доза лекарства, которую разрешается разделить на 2 приёма, не должна превышать 500 мг.
Продолжительность терапии зависит от степени тяжести заболевания, локализации очага воспаления и стадии развития недуга. Конечно, возраст пациента также имеет большое значение. Минимальный курс терапии составляет 3 дня, а максимальный – неделю (в некоторых случаях допускается приём Левофлоксацина на протяжении двух недель).
Несмотря на положительную характеристику и высокую степень эффективности препарата, он способен спровоцировать появление побочных явлений в виде:
- Тошноты и рвоты.
- Болей в голове и животе.
- Нарушений сна и отсутствия аппетита.
- Диспепсии (расстройства пищеварения) и диареи (поноса).
- Острой почечной недостаточности и артралгии.
- Мышечной слабости и разрыва сухожилий.
- Тремора (дрожания) конечностей и беспричинного чувства страха.
- Бессонницы и тревоги.
- Усиленного потоотделения и повышения уровня сахара в крови.
 Обратиться к врачу с просьбой об отмене лекарственного средства следует при появлении аллергической реакции (высыпаний на коже и сильного зуда). Принимать самостоятельное решение о необходимости использования Левофлоксацина в качестве препарата для терапии сложных и опасных заболеваний категорически запрещено. В противном случае пациент рискует спровоцировать развитие негативной реакции со стороны различных органов и систем, ухудшив своё состояние и осложнив дальнейшее лечение.
Обратиться к врачу с просьбой об отмене лекарственного средства следует при появлении аллергической реакции (высыпаний на коже и сильного зуда). Принимать самостоятельное решение о необходимости использования Левофлоксацина в качестве препарата для терапии сложных и опасных заболеваний категорически запрещено. В противном случае пациент рискует спровоцировать развитие негативной реакции со стороны различных органов и систем, ухудшив своё состояние и осложнив дальнейшее лечение.
Сравнительные характеристики
Сравнение Ципрофлоксацина и Левофлоксацина позволяет сделать правильный выбор, прежде чем принять решение о необходимости использования того или иного препарата для проведения качественной адекватной терапии. Оба лекарственных средства принадлежат к антибиотикам из ряда фторхинолонов, однако Ципрофлоксацин является препаратом первого поколения и большое количество болезнетворных бактерий смогли выработать к нему устойчивость, тогда как Левофлоксацин относится к средствам новым, обладающим повышенной эффективностью.
Главное отличие, существующее между описываемыми антибиотиками широкого спектра действия, – активное вещество:
- Препарат «Левофлоксацин» создан на основе одноимённого компонента.
- Действующий компонент Ципрофлоксацина – офлоксацин.
Под воздействие офлоксацина немногие болезнетворные бактерии погибают. Это связано с тем, что у каждой группы бактерий свой уровень чувствительности. Именно этот факт стал причиной выбора лекарства только квалифицированным врачом.
Если новейший препарат обладает прекрасной совместимостью с другими лекарственными средствами и составами, то антибиотик первого поколения под воздействием других лекарств значительно снижает уровень своей активности и концентрации. Это приводит к необходимости продлять курс терапии.
Суточную и разовую дозировку каждого антибиотика определяет лечащий врач, учитывая степень тяжести заболевания, возраст пациента, необходимость применения дополнительных лекарственных средств и локализацию очага воспаления. Не менее важно и возникновение побочных явлений, с жалобами на которые к врачам обращают в большинстве случаев пациенты, проходившие лечение с использованием Ципрофлоксацина. С этой точки зрения, Левофлоксацин обладает большей степенью безопасности, и потому чаще именно в его пользу делают свой выбор высококвалифицированные специалисты.
Для цитирования:
Белоусов Ю.Б., Мухина М.А. Клиническая фармакология левофлоксацина // РМЖ. 2002. №23. С. 1057
РГМУ
В настоящее время фторхинолоны (ФХ) рассматриваются, как важная группа химиотерапевтических препаратов в пределах класса хинолонов - ингибиторов ДНК-гиразы, характеризующихся высокой клинической эффективностью (в том числе при оральном применении), широкими показаниями к применению и составляют серьезную альтернативу другим антибиотикам широкого спектра. Создано более 15 препаратов группы ФХ, несколько новых активных соединений проходят клиническое исследование с целью получения более эффективных препаратов в отношении грамположительных микроорганизмов, микобактерий, анаэробов, атипичных возбудителей. Важной задачей является также разработка препаратов с минимальным риском побочных эффектов и высокой клинической эффективностью.
Среди ФХ в настоящее время выделяются две группы препаратов: ранние или старые (норфлоксацин, ципрофлоксацин, офлоксацин, пефлоксацин, ломефлоксацин и др.) и новые или поздние (левофлоксацин, спарфлоксацин, гатифлоксацин, гемифлоксацин и др.).
Офлоксацин применяется уже более 15 лет, обладает высокой эффективностью, хорошей переносимостью, низким уровнем побочных эффектов и отсутствием значимого межлекарственного взаимодействия. С точки зрения стереохимии офлоксацин представляет собой рацемическую смесь двух оптически активных изомеров: левовращающего (L-изомер, L-офлоксацин) и правовращающего (D-изомер, D-офлоксацин).
Левовращающий изомер офлоксацина - L-офлоксацин в настоящее время известен, как левофлоксацин (ЛФ) . Препарат был разработан в конце 1980-х годов в Японии и был предложен для применения после многоцентровых клинических испытаний, проведенных в Европе, Америке, странах Азии . В России левофлоксацин зарегистрирован и разрешен для применения в 2000 г. под торговым названием Таваник (оральная и парентеральная формы).
Левофлоксацин в 8-128 раз активнее, чем D-офлоксацин. В химической структуре ЛФ существенную роль играют две основные группы: 4-метил-пиперазинильная, обусловливающая усиление всасывания при приеме препарата внутрь, повышение его активности в отношении грамотрицательных бактерий, удлинение периода полувыведения, и оксазиновое кольцо, обусловливающее расширение спектра активности в отношении грамположительных бактерий, а также удлинение периода полувыведения. Левофлоксацин характеризуется в 2 раза большей активностью, чем офлоксацин, и, следовательно, не уступает в активности ципрофлоксацину.
Левофлоксацин обладает уникальной, почти 100% биоэквивалентностью при оральном применении. Фармакокинетический профиль ЛФ аналогичен таковому у офлоксацина. Период полувыведения составляет 4-8 часов, то есть больше, чем у ципрофлоксацина, Т max - 1,5 часа (как у ципрофлоксацина и офлоксацина), С max - 5,1 мг/л (то есть в 4 раза больше, чем у ципрофлоксацина), что практически соответствует С max при парентеральном введении в эквивалентной дозе. Левофлоксацин почти в 10 раз лучше растворяется, чем офлоксацин .
Спектр активности
Левофлоксацин, как и другие ФХ, обладает бактерицидным типом действия и широким антимикробным спектром. ФХ активны в отношении большинства энтеробактерий, грамотрицательных бацилл (гемофильной палочки, включая b
-лактамазoпродуцирующие штаммы) и грамотрицательных кокков (гоннококка, менинигококка, моракселлы, включая b
-лактамазопродуцирующие штаммы), а также синегнойной палочки. Ранние ФХ (ципрофлоксацин, офлоксацин) имеют некоторую активность в отношении стафилококков и еще меньшую - против стрептококков и энтерококков, в отличие от новых ФХ, включая левофлоксацин, высокоактивных в отношении золотистого стафилококка (за исключением метициллиноустойчивых штаммов), коагулазонегативных стафилококков, стрептококков, включая пневмококк (табл. 1, 2). Диапазон МПК ЛФ в отношении стафилококков составляет 0,06-64 мг/л (при МПК 90 0,25-16 мг/л), в отношении пневмококков диапазон МПК составляет 0,25-0,2 мг/л. Антипневмококковая активность не зависит от степени чувствительности к пенициллину. Левофлоксацин несколько менее активен в отношении энтерококков, хотя в отношении некоторых штаммов величины МПК составляют 0,5-1 мг/л. Препарат высокоактивен в отношении Listeria monocitogenes, Сorinеbacterium diphtheriae
. Внутриклеточные возбудители (хламидии, микоплазмы, легионеллы) восприимчивы ко всем ФХ. Некоторые новые ФХ активны в отношении анаэробов, ЛФ - частично . Особый интерес представляет активность ЛФ в отношении микобактерий. Изучается активность ЛФ в отношении риккетсий, бартонелл и некоторых других микроорганизмов .

В прошлом десятилетии в США была отмечена резистентность к фторхинолонам следующих патогенов: MRSA, энтерококки, Pseudomonas sp. В последующие годы докладывалось о росте резистентности сальмонелл, шигелл, Acinetobacter sp., Campilоbacter sp. и гонококка. Селекция штаммов золотистого стафилококка, устойчивых к ЛФ, наблюдается значительно реже, чем к ципрофлоксацину . Известны данные резистентности пневмококков к ФХ. Один из наиболее низких уровней устойчивости пневмококка отмечен к ЛФ (в целом 0,5% в 1997-2000 гг. в США и Канаде). Формирование резистентности к левофлоксацину возможно, однако в настоящее время устойчивость к препарату развивается наиболее медленно и не является перекрестной с другими антибиотиками .
В прошлом десятилетии в США была отмечена резистентность к фторхинолонам следующих патогенов: MRSA, энтерококки, В последующие годы докладывалось о росте резистентности сальмонелл, шигелл, и гонококка. Селекция штаммов золотистого стафилококка, устойчивых к ЛФ, наблюдается значительно реже, чем к ципрофлоксацину . Известны данные резистентности пневмококков к ФХ. Один из наиболее низких уровней устойчивости пневмококка отмечен к ЛФ (в целом 0,5% в 1997-2000 гг. в США и Канаде). Формирование резистентности к левофлоксацину возможно, однако в настоящее время .
Фармакокинетика
Левофлоксацин имеет некоторые фармакокинетические преимущества перед другими ФХ. Это определяется устойчивостью молекулы к трансформации и метаболизму в организме больного. Левофлоксацин, как и ципрофлоксацин, гатифлоксацин, тровафлоксацин и офлоксацин, существует в оральной и в парентеральной формах и может использоваться при ступенчатой терапии
, в отличие от других ФХ, доступных лишь в оральной форме.
Длительный Т 1/2 позволяет назначать ЛФ один раз в день , что повышает комплаентность пациентов . Оральная биодоступность ЛФ достигает 100% и не зависит от приема пищи, что также делает его удобным для применения. Выведение большинства ФХ происходит двойным путем (через почки и печень) . В противоположность им ЛФ выводится преимущественно через почки (90%), что требует коррекции его дозы при тяжелой почечной недостаточности. Однако отсутствие метаболизма ферментами системы цитохрома р450 обусловливают отсутствие взаимодействия с варфарином и теофиллином и других значимых лекарственных взаимодействий . В клинико-фармакологическом исследовании взаимного влияния при одновременном назначении ЛФ с нестероидными противовоспалительными, антидиабетическими, антиаритмическими средствами I и III класса, теофиллином, варфарином, циклоспорином и циметидином не отмечено (Simpson I., 1999).
Левофлоксацин подвергается метаболизму всего на 5%. Около 35% ЛФ связывается с белками сыворотки крови, и поэтому препарат хорошо распределяется в тканях . Следует подчеркнуть, что ФХ, включая ЛФ, отлично проникают в различные ткани, создавая высокие концентрации в почках, простате, женских половых органах, желчи, органах ЖКТ, бронхиальном секрете , альвеолярных макрофагах, легочной паренхиме, костях, а также в цереброспинальной жидкости, поэтому эти препараты могут широко применяться при инфекциях практически любой локализации. Кроме того, хорошее внутриклеточное проникновение обеспечивает их активность в отношении атипичных патогенов.
Клиническая эффективность ЛФ при однократном назначении 250-500 мг/сут - существенное достоинство препарата, однако при генерализованных инфекционных процессах, протекающих в тяжелой форме, ЛФ назначается дважды .
Побочные эффекты и переносимость
Побочные эффекты левофлоксацина и других ФХ известны по данным европейских и других международных исследований. В Европе исследованию подверглись более чем 5000 пациентов, в мире во время испытаний было проведено приблизительно 130 млн. назначений ЛФ.
Левофлоксацин проявил себя, как наиболее безопасный ФХ с низким уровнем гепатотоксичности (1/650000). Левофлоксацин, наряду с офлоксацином и моксифлоксацином, более безопасен в отношении патологического влияния на ЦНС. Кардиоваскулярное негативное воздействие ЛФ наблюдалось значительно реже, чем при использовании других ФХ (1/15 млн. назначений, у спарфлоксацина - в 1-3% случаев). Диарея, тошнота и рвота - наиболее частые побочные эффекты, связанные с ЛФ, однако они встречаются гораздо реже, чем у других ФХ. Частота побочных эффектов ЛФ и других ФХ представлена в табл. 3 .

Показано, что увеличение дозы ЛФ до 1000 мг/сут не приводит к росту числа побочных эффектов, а их вероятность не зависит от возраста пациента .
В целом уровень побочных реакций, связанных с ЛФ, наиболее низкий среди ФХ, а переносимость ЛФ может быть расценена, как очень хорошая .
Левофлоксацин при инфекциях нижних дыхательных путей
Внебольничная пневмония
Внебольничная пневмония - одно из наиболее распространенных заболеваний с серьезным прогнозом. Заболеваемость пневмонией в Европе колеблется от 2 до 15 случаев на 1000 человек в год. По данным А.Г. Чучалина, распространенность пневмоний среди взрослого населения России составляет 5-8 на 1000 человек . В США ежегодно регистрируется 2-3 млн. случаев внебольничной пневмонии, по поводу которых совершается около 10 млн. врачебных визитов в год . По данным ЦНИИОИЗ МЗ РФ, ежегодно в России переносят пневмонию более 1,5 млн. взрослых.
Общая летальность при пневмонии составляет около 20-30 случаев на 100 тыс. человек в год. Смертность среди амбулаторных больных с низкой степенью риска не более 1%, а у больных, госпитализированных с пневмонией - до 14% (у критических больных до 30-40%) (Fine et al. 1999).
Пневмококк остается наиболее частым возбудителем внебольничных пневмоний - 30,5% (20-60%). В молодых и средних возрастных группах часто встречаются Mycoplasma pneumoniae (5-50%) и Chlamydia pneumoniae (5-15%). В старших возрастных группах эти возбудители встречаются реже (1-3%). Легионелла - редкий возбудитель пневмонии (4,8%), однако она вызывает до 10% случаев тяжелых пневмоний. Легионеллезная пневмония занимает второе место по летальности после пневмококковой. H. influenzae чаще вызывает пневмонию у курильщиков или на фоне хронического бронхита (3-10%) и, по некоторым данным, в России занимает второе место в этиологии тяжелых пневмоний. Представители семейства Enterobacteriaceae (E.coli, K.pneumoniae ) встречаются у пациентов с факторами риска (сахарный диабет, недостаточность кровообращения и др.) в 3-10% случаев. Moraxella сatarrhalis выделяется в 0,5% случаев Сравнительно редко выделяют Str. pyogenes, Chl. psittaci, Coxiella burnetii и др. При тяжелой пневмонии относительно большую долю среди бактериальных агентов занимает золотистый стафилококк, вероятность его обнаружения возрастает с возрастом или после перенесенного гриппа (3-10%), при этом уровень летальности может достигать 50%. В 50% случаев выделить возбудитель не удается, а в 2-5% случаев выявляется микст-инфекция.
На протяжении последних лет во всем мире наблюдается стремительный рост резистентности возбудителей пневмонии к антибактериальным препаратам . Значительно увеличилась доля пневмоний, вызываемых штаммами пневмококка, устойчивыми к пенициллину (до 51,4%) и цефалоспоринам, а также к макролидам (к эритромицину до 45,9%), тетрациклинам и ко-тримоксазолу. При этом в некоторых регионах резистентность к макролидам превалирует над устойчивостью к пенициллину. В некоторых странах частота устойчивости пневмококков к пенициллину может достигать 60%. Масштабных исследований резистентности пневмококков к пенициллину в нашей стране не проводилось. По данным локальных исследований в Москве, частота устойчивых штаммов составляет 2%, штаммов с промежуточной чувствительностью - около 20%. Устойчивость пневмококков к пенициллину связана не с продукцией b -лактамаз, а с модификацией мишени антибиотика в микробной клетке - пенициллин-связывающих белков, поэтому ингибитор-защищенные пенициллины в отношении этих пневмококков также неактивны. Устойчивость пневмококков к пенициллину обычно cопровождается устойчивостью к цефалоспоринам I-II поколений, макролидам, тетрациклинам, ко-тримоксазолу.
Проблема устойчивости пневмококка к антибиотикам в России пока не столь актуальна, как на Западе, однако следует помнить, что резистентность штаммов варьирует в каждом регионе. Факторами риска для развития резистентности являются пожилой и детский возраст, сопутствующие заболевания, предшествующая антибиотикотерапия, пребывание в домах ухода.
Резистентность гемофильной палочки к пенициллинам достигает 10%, растет ее резистентность к новым макролидам.
Антибактериальная терапия пневмоний, в подавляющем большинстве случаев эмпирическая, требует применения препаратов с широким спектром действия. При выборе способа лечения учитывают степень тяжести заболевания и факторы риска. Эмпирическая терапия всегда должна охватывать пневмококк, необходимо рассматривать применение антибиотиков, активных в отношении микоплазмы и легионеллы, во время эпидемии гриппа - S. aureus , а у пожилых больных - Enterobacteriaceae. Общепринято при тяжелой внебольничной пневмонии начинать лечение комбинацией антибиотиков, состоящей из макролида и средства, активного в отношении грамотрицательных энтеробактерий, например цефалоспорина. Кроме того, современные руководства рекомендуют применять новейшие ФХ для лечения внебольничных пневмоний, требующих госпитализации.
Фторхинолоны обладают широким спектром антимикробной активности. Эти препараты проявляют природную активность в отношении практически всех потенциальных возбудителей внебольничной пневмонии. Однако применение ранних ФХ (ципрофлоксацин, офлоксацин, пефлоксацин) при внебольничной пневмонии было ограничено из-за их слабой природной активности в отношении основного возбудителя пневмонии - S. pneumoniae . Значения минимальных подавляющих концентраций (МПК) ранних ФХ в отношении пневмококка составляют от 4 до 8 мкг/мл, а их концентрация в бронхолегочной ткани значительно ниже, что недостаточно для успешной терапии. Описаны случаи, когда терапия ФХ при пневмококковой пневмонии не приносила успеха. По другим данным, возможно создание высокой тканевой концентрации этих препаратов, достаточной для адекватной противопневмококковой активности. Это подтверждается клинико-бактериологической эффективностью ципрофлоксацина при лечении пневмоний и других инфекций нижних дыхательных путей, не уступающей стандартной терапии b -лактамными антибиотиками. Доказанная эффективность ФХ при инфекции нижних дыхательных путей позволяет определить их место при лечении внебольничной пневмонии. У больных моложе 65 лет, не курящих, без серьезных хронических заболеваний возбудителем внебольничной пневмонии в 80% случаев является пневмококк и другие стрептококки, реже атипичные микроорганизмы. Фторхинолоны у этой категории больных являются альтернативой для лечения среднетяжелой и тяжелой пневмонии, например, при аллергии на пенициллины. У больных старше 65 лет, злостных курильщиков, страдающих серьезными хроническими соматическими заболеваниями, алкоголизмом возбудителями пневмонии являются преимущественно грамотрицательные патогены, а именно H. influenzae, M. сatarrhalis, Klebsiella spp. , в трети случаев пневмококк, часто атипичные патогены. Фторхинолоны являются препаратами выбора у данной категории больных, особенно при амбулаторном лечении, поскольку могут назначаться в оральной форме при среднетяжелом течении заболевании с однократным приемом в сутки, что повышает комплаентность пожилых пациентов . При лечении пневмоний, требующих госпитализации, преимуществом ФХ является возможность использования ступенчатой терапии, что существенно улучшает фармакоэкономические аспекты лечения .
На фоне роста устойчивости ключевых возбудителей респираторных инфекций к антибиотикам (в частности, распространение штаммов S.pneumoniae , резистентных к пенициллину и макролидам) особое положение приобретают новые или так называемые респираторные фторхинолоны (левофлоксацин, моксифлоксацин, гатифлоксацин). Новые ФХ обладают повышенной, в сравнении с классическими фторхинолонами (офлоксацином, ципрофлоксацином), активностью в отношении S.pneumoniae . Необходимо также подчеркнуть, что высокая антипневмококковая активность новых ФХ наблюдается независимо от чувствительности пневмококка к пенициллину и/или к макролидам . Так же очевидно превосходство новых ФХ и в отношении атипичных возбудителей (M.pneumoniae, C. pneumoniae, L.pneumophila ). И, наконец, эти антибиотики «унаследовали» высокую активность классических ФХ против H.influenzae и M.catarrhalis . Не вызывает сомнений, что новые ФХ являются приемлемой альтернативой макролидам, амоксициллину/клавуланату и пероральным цефалоспоринам в лечении внебольничной пневмонии. К очевидным достоинствам новых ФХ следует добавить возможность приема один раз в сутки и использование их в рамках ступенчатой терапии .
В проведенных к настоящему времени исследованиях, включавших в т.ч. и больных с тяжелым и (или) прогностически неблагоприятным течением заболевания, были получены убедительные свидетельства превосходящей или, по меньшей мере, сопоставимой клинической и микробиологической эффективности монотерапии ЛФ по сравнению с традиционным комбинированным лечением (цефалоспорины + макролиды). Это обстоятельство, а также прекрасный профиль безопасности, подтвержденный многолетней практикой широкого клинического применения, и очевидные экономические преимущества монотерапии объясняют присутствие ЛФ в современных схемах лечения внебольничной пневмонии. Левофлоксацин занимает видное место в современных схемах лечения взрослых пациентов с внебольничной пневмонией , не подлежащих госпитализации (Frias J., 1998; Bartlett J.G., 2000), а также в условиях стационара (Frias J., 2000; Mandell L.A., 1997)
При внебольничной пневмонии клиническая эффективность ЛФ превосходила эффективность терапии цефтриаксоном, цефуроксимом (в т.ч. в сочетании с эритромицином или доксициклином) и составила 96 и 90%, бактериологическая эффективность - 98 и 85% соответственно; различия были статистически достоверны (File T.M.,1997).
По данным I. Нarding (2001), левофлоксацин был более эффективным при лечении внегоспитальной пневмонии, чем кларитромицин, бензилпенициллин, цефтриаксон, амоксициллин/клавулановая кислота.
В ходе рандомизированного, двойного слепого, мультицентрового исследования у 518 больных внебольничной пневмонией проводился сравнительный анализ клинической эффективности применения ЛФ и амоксициллина/клавуланата. Клиническая эффективность при приеме 500 мг ЛФ 1 раз в сутки составила 95,2%, при приеме ЛФ по 500 мг 2 раза в сутки - 93,8%, а при приеме амоксициллина/клавуланата по 625 мг 3 раза в сутки - 95,3% .
В многоцентровом открытом рандомизированном исследовании сравнивалась эффективность ЛФ и цефтриаксона в комбинации с эритромицином у больных внебольничной пневмонией с высоким риском неблагоприятного исхода. 132 больным, получавшим ЛФ, препарат изначально вводился внутривенно (500 мг 1 раз в сутки), затем перорально в той же дозе в течение 7-14 дней. В группе сравнения 137 пациентов получали внутривенно или внутримышечно цефтриаксон (1-2 г 1 раз в сутки) и внутривенно эритромицин (500 мг 4 раза в сутки) с последующим переходом на пероральный прием амоксицилина/клавуланата (875 мг 2 раза в сутки) совместно с кларитромицином (500 мг 2 раза в сутки). Клиническая эффективность в 1 группе была 89,5%, во 2 группе - 83,1%. Таким образом, монотерапия ЛФ не уступает по эффективности традиционному комбинированному лечению у больных с высокой вероятностью летального исхода.
В ходе другого мультицентрового рандомизированного исследования у 456 больных внебольничной пневмонией (1 группа - 226 пациентов получали левофлоксацин, 2 группа 230 пациентов получали цефтриаксон и/или цефуроксим аксетил) была изучена клиническая и микробиологическая эффективность ЛФ, вводимого внутривенно (500 мг 1 раз в сутки) и/или перорально (500 мг 1 раз в сутки), в сравнении с цефтриаксоном, вводимым внутривенно (1,0-2,0 г 1-2 раза в сутки) и/или цефуроксимом аксетилом, вводимым перорально (500 мг 2 раза в сутки). Помимо этого, исходя из конкретной клинической ситуации, 22% больных второй группы назначался эритромицин перорально (1 г 4 раза в сутки). Клиническая и микробиологическая эффективность монотерапии ЛФ оказалась достоверно выше традиционной схемы лечения. Так клинический успех у пациентов 1 группы составил 96%, у пациентов 2 группы - 90%, а частота эрадикации возбудителя у микробиологически обследованных пациентов - 98% и 85%, соответственно.
Роль и место ЛФ в рамках ступенчатой терапии внебольничной пневмонии в сравнении с традиционной терапией были изучены в рамках масштабного канадского исследования (CAPITAL Study ), включавшего 1743 больных . Для решения вопроса о месте лечения и способе введения лекарственного средства использовалась шкала M.J. Fine et al., 1997. Если итоговая оценка пациента не превышала 90 баллов, то лечение проводилось в домашних условиях с назначением ЛФ (500 мг 1 раз/сутки, внутрь) в течение 10 дней. Если же итоговая оценка составляла 91 и более баллов, то больного госпитализировали и первоначально ЛФ (500 мг 1 раз/сут) вводили внутривенно. По достижении стабильного состояния (способность проглатывать пищу, отрицательные результаты посевов крови, температура тела 38,0°C, частота дыхания <24/мин, частота сердечных сокращений <100/мин), лечение продолжалось с назначением оральной формы ЛФ (500 мг 1 раз/сутки). Использовали унифицированные критерии для выписки больного из стационара: возможность приема антибиотика внутрь; число лейкоцитов периферической крови < 12x109/л; стабильное течение сопутствующих заболеваний; нормальная оксигенация крови.
В результате не было отмечено достоверных различий по частоте повторных госпитализаций, летальности и качеству жизни среди больных, получавших ЛФ в рамках ступенчатой терапии, или при стандартном лечении. Одновременно внедрение ступенчатой терапии ЛФ привело к уменьшению на 18% койко-дней по данной нозологической форме и сокращению расходов на 1700 $ США (из расчета на одного больного).
Клиническую эффективность и безопасность ЛФ и некоторых новых макролидов (азитромицин, кларитромицин) при лечении внебольничной пневмонии сравнивали с помощью мета-анализа рандомизированных контролируемых исследований. Частота полного клинического выздоровления была явно выше при применении ЛФ (78,9%), чем макролидов (азитромицин - 57%, кларитромицин 63,3%). Была отмечена более высокая частота развития нежелательных лекарственных явлений при применении ЛФ - 36,6% (азитромицин - 12,6%, кларитромицин - 27,1%), но, по мнению авторов, профиль безопасности ЛФ практически не отличается от макролидов, и левофлоксацин может быть рекомендован в качестве эффективного средства при лечении внебольничной пневмонии.
Представленные данные позволяют сделать вывод, что клиническая и микробиологическая эффективность монотерапии левофлоксацином не меньше, чем у традиционных схем лечения внебольничной пневмонии .
Большое количество исследований подтвердило не только клиническое преимущество ЛФ, но и его экономическое превосходство над другими антибактериальными препаратами.
В исследовании, проведенном в Tалахасском медицинском центре, было показано экономическое преимущество использования ЛФ при лечении внебольничной пневмонии в сравнении с традиционной парентеральной терапией. Предполагаемая экономия составила в среднем 111$ на пациента.
В многоцентровом рандомизированном контролируемом исследовании, проведенном в 19 канадских больницах, был оценен экономический результат лечения взрослых пациентов с внебольничной пневмонией. Больницы были разделены на две группы: использующие исследуемый подход и использующие обычную стандартную терапию. Исследуемый способ ведения включал применение ЛФ, как антибиотика выбора, и использование индекса тяжести пневмонии PSSI (Pneumonia Severity Scoring Index), в соответствии с которым пациенты распределялись на 5 классов и решался вопрос о способе лечения (амбулаторно или в стационаре). В больницах, использующих обычный подход, решение о госпитализации, о выборе антибиотика (за исключением ЛФ) и другие решения принимали лечащие врачи. В анализ было включено 716 пациентов по исследуемому способу и 1027 пациентов по общепринятой терапии. В больницах с исследуемым способом было меньше госпитализаций, чем в больницах с обычной терапией (46,5% и 62,2% соответственно, р =0,01), также отмечалось сокращение сроков нахождения больных в стационаре в среднем на 1,6 дня и экономия 457-994 долл. на пациента, без снижения клинической эффективности и качества жизни.
Исследование, проведенное системой здравоохранения INOVA, показало, что левофлоксацин - это экономически выгодная альтернатива ципрофлоксацину при инфекционных заболеваниях различной локализации (верхних и нижних дыхательных путей, мочевыводящего тракта, кожи и мягких тканей и др.) и что использование критериев риска заболевания (PSI) может уменьшить частоту оправданных госпитализаций при внебольничной пневмонии, что также ведет к экономии средств. К тому же опыт продемонстрировал экономическое и клиническое преимущество применения ступенчатой терапии.
В другое крупное мультицентровое проспективное открытое рандомизированное, активно контролируемое исследование III фазы было включено 310 амбулаторных и 280 стационарных больных с внебольничной пневмонией, которым назначали левофлоксацин или цефуроксим аксетил (внутривенно или перорально). Экономическая оценка проводилась только для амбулаторных больных. Было установлено, что экономическое преимущество ЛФ достигает 233 $ на пациента (р=0,008).
В исследовании, проведенном в Онкологическом центре Техасского университета доказано, что использование левофлоксацина безопасно, эффективно и экономически выгодно при лечении внебольничной пневмонии у взрослых в сравнении с b -лактамными антибиотиками, а также кларитромицином. В данном исследовании проводилось определение чувствительности к исследуемым антибиотикам с использованием МПК и был выявлен высокий уровень резистентности основных возбудителей пневмонии (пневмококка, гемофильной палочки, моракселлы) к b -лактамам, рост резистентности атипичных патогенов к макролидам и, в противоположность этому, низкий уровень резистентности к ЛФ. Частые случаи возникновения аллергических реакций на b -лактамы в сравнении с ЛФ и хорошая переносимость последнего также показали его преимущество. Во втором исследовании рассматривался вопрос об оптимальной антибактериальной терапии при внебольничной пневмонии у пациентов с различными сопутствующими состояниями (ХНЗЛ, диабет, хроническая сердечная недостаточность, алкоголизм, нахождение в домах престарелых, работа на животноводческих фермах и т.д.). В результате среди всех ФХ для ведения внебольничной пневмонии был рекомендован только левофлоксацин.
В следующем исследовании изучалась замена левофлоксацином других ФХ при пневмонии и инфекциях другой локализации. Производилось микробиологическое исследование, клиническая и фармакоэкономическая оценки. В результате замена более дорогим препаратом (левофлоксацином) более дешевых (офлоксацина, ципрофлоксацина) оказалась более выгодной.
Хронический бронхит в фазе обострения
Согласно результатам исследования C.A. DeAbate (1997), клиническая и бактериологическая эффективность ЛФ при приеме в дозе 500 мг 1 раз в сутки в течение 5-7 дней сопоставима с 7-10-дневным приемом цефуроксима в дозе 250 мг 2 раза в сутки. Клиническая эффективность составила 94,5 и 92,6%, бактериологическая - 97,4 и 92,6%, соответственно.
Согласно данным M.P. Habib (1998), клиническая и бактериологическая эффективность однократного приема 500 мг ЛФ в течение 5-7 дней сопоставима с 7-10-дневным приемом цефаклора в дозе 250 мг 3 раза в сутки. Клиническая эффективность составила 91,6 и 85%, бактериологическая - 94,2 и 86,5%, соответственно .
Нозокомиальная пневмония
В этиологии нозокомиальной пневмонии преобладает грамотрицательная флора (Klebsiella sp., P. mirabilis, E. coli, H. influensae, P. aeruginosa ). Из грамположительной флоры встречаются S. aureus , реже пневмококки, часто полирезистентные штаммы. Фторхинолоны давно успешно используются при лечении данной патологии. Учитывая антимикробный спектр ЛФ, назначение его при нозокомиальной пневмонии может быть вполне оправдано. Однако при предполагаемой или при подтвержденной инфекции P. аeruginosa требуется комбинированная антибактериальная терапия обычно с антисинегнойными b -лактамными антибиотиками для предупреждения развития резистентности.
Заключение
Опыт применения левофлоксацина убедительно доказывает, что это высокоэффективный препарат, сопоставимый по степени эффективности с другими новыми фторхинолонами. Практически в равной степени левофлоксацин эффективен в отношении как грамположительной, так и грамотрицательной аэробной флоры, а также обладает высокой активностью в отношении атипичных возбудителей. Левофлоксацин имеет практически идеальные фармакокинетические параметры и две лекарственные формы, оральную и парентеральную, что позволяет максимально оптимизировать дозы и схемы терапии и применять его в рамках супенчатой терапии. Высокая бактерицидная активность левофлоксацина в сочетании с высокими значениями максимальных концентраций, хорошим проникновением в ткани, показателями AUC обеспечивает максимальный терапевтический эффект.
Среди других препаратов группы ФХ левофлоксацин обладает наилучшей переносимостью с низким уровнем побочных эффектов.
В настоящее время левофлоксацин с успехом применяется в основном при инфекциях нижних дыхательных путей. Однако, учитывая широкий антимикробный спектр, оптимальные фармакокинетические параметры, хорошую переносимость, левофлоксацин может применяться при инфекциях практически любой локализации (синуситы, инфекции мочевыводящих путей, кожи и мягких тканей, малого таза, интраабдоминальные инфекции, тяжелые генерализованные инфекции, кишечные инфекции, инфекции, передающиеся половым путем, и др.).
Формирование резистентности к левофлоксацину возможно, однако в настоящее время устойчивость к препарату развивается наиболее медленно и не является перекрестной с другими антибиотиками.
Наряду с высокой клинической эффективностью левофлоксацин несомненно обладает фармакоэкономическими преимуществами, что актуально в условиях современной системы здравоохранения.
Литература:1. Tenover FC, Hughes JM. The challenges of emerging infectious diseases: Development and spread of multiple-resistans bacterial pathogens. JAMA 1996;275:300-304.
2. Report pf the ASM Task Force on Antibiotic Resistance. American society for microbiology. Antimicrob agent chemother 1995; 39(sappl); 2-23.
3. Rockefeller University Workshop. Special Report. Multiple-resistans bacterial pathogens. N Engl J Med 1994;330:1247-1251.
4. Bartlett JG, Breiman RF, Mandell LA, File TM Jr. Guidelines from the infections Diseases Sosiety of America. Community- acquired pneumonia in adults: guidelines for management. Clin infect Dis 1998;;811-838.
5. Niederman MS, Bass JB Jr, Campbell GD, et al. Guidelines for the initial management of adults with community- acquired pneumonia: Diagnosis, assessment of severity, initial antimicrobial therapy.; 1993;14181426.
6. Davis R, Bryson HM, Levofloxacin: a review of its antibacterial activity, farmacokinetics and therapeutic efficasy. Drags 1994;47;677-700.
7. Cunha BA, Community- acquired pneumonia cost-effective antimicrobial therapy. Postgrad Med 1996;99:109-122.
8. Hayakawa Y, Furuhama K, Takayama S, Osada Y, Levofloxacin a new quinolone antibacterial agent. Arzneim Forsch Drag Res 1992;42:363-364.
9. Nacamori Y, Miyashita Y, Nacatu K, Levofloxacin; Penetration into sputum and once-daily treatment of respiratory tract infection. Drags 1995;49(sappl 2):418-419.
10. Shishido H, Furukawa K, Nagai H, Kawakami K, Kono H, Oral levofloxacin 500mg and 300mg daily doses in difficult-to-treat respiratory infections. Drags 1995;49(sappl 2):433-435.
11. Kawai T, Clinical evaluation of levofloxacin 200mg 3 times daily in the treatment of bacterial lower respiratory tract infections. Drags 1995(sappl 2):416-417.
12. Klugman KP, Capper T, Levofloxacin in vitro activity and sinergistic activity in combination with other antibacterials against antibioticresistans S. Pneumonia, and selections of resistans mutants. 1995:87.
13. Marcus A, Isert D, Klesel N, Selbert C Killing activity of levofloxacin and ciprofloxacin against S. pneumonia in vitro and vivo. 1995:90.
14. File TM, Segreti J, Dunbar L et al. A multicenter, randomized study comparing the efficacy and safety IV and/or oral levofloxacin versus ceftriaxon and/or cafuroxim axetil in treatment of adults with community- acquired pneumonia. Antimicrob Agent Chemother 1997;41:1965-1972.
15. Sydnor TA, Scheld WM, Gwaltney JM. A noncomparative study to evaluate the safety and efficasy of levofloxacin in the treatment of acute bacterial sinusitis in adults. 1995.
16. File TM Fluoroquinolones and respiratory tract infections. Infect Dis Clin Pract. 19979Sappl 2):559-566.
17. Chein SC, Rogge MC, Gisclon LG, et al. Pharmokinetic profil of levofloxacin following once-daily 500mg oral or IV doses. Antimicrob Agent Chemother 1997;47:2256-2260.
18. Niederman MS, McCombs JS, Unger AN, et al. The cost of treating community- acquired pneumonia. Clin Ther. 1998;20:820-837.
19. Isaacson DM, Fernandes JA, Frosco M et al. Levofloxacin: a review of its antibacterial activity. 1996;1:391-439.
20. Cooper I, Isbell DJ, Kruszinsky JA et al. Comparative in vitro activity of L-ofloxacin and FK037 to other agents against 10,040 fresh clinical isolates. Int J Antimicrob Agents. 1996;6:201-211.
21. DeAbate CA, Russel M, McElvaine P et al. Safety and efficasy of levofloxacin versus cefuroxime axetil in acute bacterial exacerbation of chronic bronhitis. Respir Care.1997;42:206-13.
22. Biedenbah DJ, Jones RN. The comparative antimicrobial activity of levofloxacin tested against 350 clinical isolates streptococci. Diagn Microbiol Infect Dis. 1996;25:47-51.
23. Hazlet TK, Hu TW. Assotiation between formulary strategies and hospital drag expenditures. Am J Hosp Pharm 1992;49:2207-10.
24. Guay DRP, Sequential antimicrobial therapy; a realistic approach to cost conteinment? Pharmacoeconomics 1993;3:341-4.
25. Acar JF, Goldstain FW. Trends in bacterial resistense to fluoroquinolones. Clin Infect Dis1997;24:567-73.
26. Segreti J, Goots TD, Goodman LJ et al. High-level quinolone resistense in clinical isolates of Campilobacter jejuni. J Infect Dis 1992;165:667-70.
27. Smith SM, Eng RHK, Bais P, Fan-Haward P, Texon-Tuman F. Epidemiology of ciprofloxacin resistence among patient with meticillin-resistant S. aureus. J Antimicrob Chemother 1990;26:567-72.
28. Selman LJ, Mayfield DC, Thornsberry C et al. Risc factors associated with antimicrobial resistance among Str. Pneumonia in the USA.2000.
29. Kim MK, Nightingale CH. Pharmacokinetik and pharmacodinamic of the phluoroquinolones. In: Andriole VT, ed. The quinolones, 3rd ed San Dieg: Academic Press , 2000:169-202.
30. Gwailtneiy JM Jr Acute community-asqued sinusitis. Clin Infect Dis 1996;23:1209-25.
31. Bartlett JG, Dowell SF, Mandell LA, File TM Jr, Musher DM, Fine AM. Practice guidelines for the management of community-asqued pneumonia in adults. Clin Infect Dis 2000; 31:1209-25
32. Grossman RF. The role of the fluoriquinolones in respiratory infections. J Antimicrob Chemother 1997;40(sapplA):59062
33. Hooton TM, Stamm WE. Diagnosis and treatment of uncomlicated urinary tract infetions. Infect Dis Clin North Am 1997;11:551-81.
34. Bergeron MG. Treatment of pyelonephritit in adults. Med Clin North AM 1995;79:619-49.
35. Nickel JC. Practical approach to the management of prostatitis. Techniques Urol 1995;1:162-7.
36. Karchmer AW. Use of quinolones in skin and skin structure and other infections. 2000.
37. Ortho-McNeil Pharmaceutical. Levofloxacin tablets-injection package insert. Raritan, NJ;2000.
38. Hamer DH, Gorbach SL. Use of the quinolones for treatment and prophilaxis of bacterial gastrointestinal infections. In Andriole VT, ed. The quinolones 3rd ed. San Diego: Academic Press, 2000:303-23.
39. Weigelt J, Brasel K, Faro S. Use of quinolones in surgery and obstetrics and genicology. JN: Andriole VT, ed. The quinolones, 3rd ed. San Diego:Academic Press, 2000:285-301.
40. Levison ME, Bush LM. Peritonitis and other intra-abdominal infections.1995.
41. Guay DRP. Implications of quinolones pharmacocinetic drag interactions. Hosp Pharm 1997; 32:677-90.
42. Fish DN. Fluoroquinolones adverse effects and drag interactions. Pharmacotherapy 2002;21(10pt2);2535-72.
43. Lipsky BA, Baker CA. Fluoroquinolones toxiticy prophil; a review focusing on newer agents. Clin Infect Dis 1999;28:352-64.
44. Jones RN, Pfaller MA. Bacterial resistance: a worldwide problem. Diagn Microbiol Infect Dis 1998;31:379-88.
45. Guay DRP. Quinolones. Antimicrobial therapy in the elderly patient. New York/ 1994: 237-310.
46. Падейская Е. Н., Яковлев В.П. Антимикробные препараты группы фторхинолонов в клинической практике. М.: Логата, 1998.-351с.
47. Яковлев В.П., Литовченко К.В. Левофлоксацин-новый препарат группы фторхинолонов.// Инфекция и антимикробная терапия, 2001; 3 (5): 132-140.
48. Экономическая оценка эффективности лекарственной терапии (фармакоэкономический анализ). Под ред. проф. Воробьева П.А.// Ньюдиамед, М. - 2000.
49. Навашин С.М., Чучалин А.Г., Белоусов Ю.Б. и др. Антибактериальная терапия пневмоний у взрослых. Учебно-методическое пособие для врачей. М. - 1998.
50. Синопальников А.И., Дуганов В.К. Левофлоксацин: ступенчатая терапия внебольничной пневмонии у взрослых // Русский медицинский журнал. 2001. № 15. с. 3-10.
51. Стандарты (протоколы) диагностики и лечения больных с неспецифическими заболеваниями легких (Приложение к приказу № 300 Минздрава России). М. 1999. Универсум Паблишинг. 47 с.
52. Чучалин А.Г. Болезни органов дыхания. Медицинская газета. - 2000. № 43. С. 8-9.
53. Яковлев С.В. Новое поколение фторхинолонов - новые возможности лечения внебольничных инфекций дыхательных путей // Антибиотики и химиотерапия. 2001. Т. 46. № 6. С. 38-42
54. Carbon C., Ariza H., Rabie W.J., et al. Comparative study of levofloxacin and amoxycillin/clavulanic acid in adults with mild-to-moderate community-acquired pneumonia. Clin Microbiol Infect 1999; 5: 724-32.
55. Mandell L.A., Marrie T.J., Grossman R.F. et al. Canadian guidelines for the initial management of community-acquired pneumonia: an evidence-based updat
Catad_tema Мочеполовые инфекции - статьи
Офлоксацин в урологической практике
В.Е. Охриц, Е.И. Велиев
Кафедра урологии и хирургической андрологии РМАПО
Антибактериальные препараты (АБП) класса фторхинолонов (ФХ), объединенные общим механизмом действия (ингибирование синтеза ключевого фермента бактериальной клетки – ДНК-гиразы), в настоящее время занимают одну из ведущих позиций в химиотерапии бактериальных инфекционных заболеваний. Первый хинолон был получен случайно в процессе очистки противомалярийного препарата хлорохина. Это была налидиксовая кислота, которая более 40 лет применялась для лечения инфекций мочевых путей (ИМП). В последующем введение атома фтора в структуру налидиксовой кислоты положило начало новому классу АБП – ФХ. Дальнейшее совершенствование ФХ привело к появлению в середине 1980-х годов монофтор-хинолонов (содержащих один атом фтора в молекуле): норфлоксацина, пефлоксацина, офлоксацина и ципрофлоксацина.
Спектр действия ФХ
Все ФХ являются препаратами широкого спектра действия, который включает бактерии (аэробные и анаэробные, грамположительные и грамотрицательные), микобактерии, хламидии, микоплазмы, риккетсии, боррелии, некоторые простейшие.
ФХ характеризуются активностью в отношении преимущественно грамотрицательных бактерий : семейств Enterobacteriaceae (Citrobacter, Enterobacter, Escherichia coli, Klebsiella, Proteus, Providencia, Salmonella, Shigella, Yersinia), Neisseriae, Haemophilus, Moraxella, в отношении которых минимальная подавляющая концентрация (МПК90)
ФХ в большинстве случаев составляет Среди ФХ имеются различия в активности против разных групп микроорганизмов и отдельных видов бактерий. Наиболее активными in vitro ФХ являются ципрофлоксацин (в отношении Enterobacteriaceae и Pseudomonas aeruginosa) и офлоксацин (в отношении грамположительных кокков и хламидий).
Резистентность бактерий к ФХ развивается относительно медленно, в основном она связана с мутациями генов, кодирующих ДНК-гиразу или топоизомеразу IV. Другие механизмы резистентности бактерий к ФХ связаны с нарушением транспорта препаратов через пориновые каналы во внешней клеточной мембране микробной клетки или с активацией белков выброса, которые приводят к выведению ФХ из клетки.
Фармакокинетика ФХ
Все ФХ хорошо всасываются в желудочно-кишечном тракте, достигая максимальных концентраций в крови через 1–3 ч; прием пищи несколько замедляет всасывание, но не влияет на его полноту. ФХ характеризуются высокой биодоступностью при приеме внутрь, которая у большинства препаратов достигает 80–100% (за исключением норфлоксацина – 35–45%).
Все ФХ длительно циркулируют в организме в терапевтических концентрациях (период полувыведения 5–10 ч), благодаря чему применяются 1–2 раза в сутки.
Концентрации ФХ в большинстве тканей организма сопоставимы с сывороточными или превышают их; в большой концентрации ФХ накапливаются в паренхиме почек и в ткани простаты. Отмечается хорошее проникновение ФХ в клетки – полиморфно-ядерные лейкоциты, макрофаги, что важно при лечении внутриклеточных инфекций.
Имеются различия по выраженности метаболизма, которому подвергаются ФХ в организме. В наибольшей степени биотрансформации подвержен пефлоксацин (50–85%), в наименьшей – офлоксацин (менее 10%, при этом 75–90% офлоксацина в неизмененном виде выводится почками).
Важным достоинством ФХ является наличие у ряда препаратов (офлоксацин, пефлоксацин, ципрофлоксацин) двух лекарственных форм – для приема внутрь и для парентерального применения. Это делает возможным применять их последовательно (ступенчатая терапия), начиная с внутривенного введения и затем переходя на прием препаратов внутрь, что, безусловно, повышает комплайнс и экономическую обоснованность лечения.
Переносимость ФХ
В целом ФХ хорошо переносятся, хотя у 4–8% пациентов они могут вызывать нежелательные эффекты (наиболее часто – со стороны желудочно-кишечного тракта, центральной нервной системы и кожи).
Приблизительно 20 лет назад в исследованиях на животных была выявлена способность ФХ вызывать артропатии, что послужило причиной фактического запрета на использование ФХ у беременных и детей младше 12 лет. Назначение ФХ пациентам этих категорий возможно только по жизненным показаниям. В публикациях, касающихся применения ФХ у тяжело больных детей, не были подтверждены данные о частом развитии артротоксического эффекта. Он был отмечен менее чем у 1% детей и зависел от возраста и пола: встречался чаще у подростков, чем у детей раннего возраста, и у девочек чаще, чем у мальчиков.
Одним из самых безопасных ФХ считается офлоксацин . По данным некоторых исследователей при долгосрочном наблюдении за детьми и подростками, получавшими офлоксацин по жизненным показаниям, случаев артротоксичности (как острой, так и кумулятивной) выявлено не было. Кроме того, у больных с сопутствующими заболеваниями суставов не отмечалось обострения на фоне приема офлоксацина.
Особенности офлоксацина
Офлоксацин можно рассматривать как один из наиболее высокоактивных для лечения ИМП препаратов из ранних ФХ. Благодаря своей структуре и механизму действия офлоксацин обладает высокой бактерицидной активностью. Препарат активен в отношении грамотрицательных и грамположительных микроорганизмов (включая штаммы, резистентные к другим АБП), а также внутриклеточных возбудителей.
Офлоксацин можно назначать одновременно со многими АБП (макролидами, b-лактамами). Благодаря этому свойству препарат широко используют в составе комбинированной терапии при инфекционных заболеваниях. Офлоксацин в отличие от ципрофлоксацина сохраняет активность при одновременном применении ингибиторов синтеза РНК-полимеразы (хлорамфеникола и рифампицина), так как он практически не метаболизируется в печени.
Биодоступность офлоксацина при пероральном приеме и парентеральном введении идентична. Благодаря этому при замене инъекционного пути введения препарата пероральным коррекции дозы не требуется (одно из существенных отличий офлоксацина от ципрофлоксацина). Офлоксацин назначают 1–2 раза в сутки. Прием пищи не влияет на его всасываемость, однако при употреблении жирной пищи всасывание офлоксацина замедляется.
Офлоксацин хорошо проникает в органы-мишени (например, при хроническом простатите – в ткань предстательной железы). Между используемой дозой офлоксацина и его концентрацией в тканях существует линейная зависимость. Препарат выделяется преимущественно почками (более 80%) в неизмененном виде.
Офлоксацин в меньшей степени, чем ципрофлоксацин, взаимодействует с другими препаратами, практически не влияет на фармакокинетику теофиллина и кофеина.
Активность офлоксацина в наибольшей степени выражена в отношении грамотрицательных бактерий и внутриклеточных патогенов (хламидий, микоплазм, уреаплазм), в отношении грамположительной флоры и синегнойной палочки офлоксацин менее активен. Бактерицидный эффект офлоксацина проявляется достаточно быстро, а резистентность микроорганизмов к нему развивается медленно. Это обусловлено его влиянием на один ген ДНК-гиразы и на топоизомеразу IV. Основные отличия офлоксацина от других ФХ (Яковлев В.П., 1996):
1. Микробиологические:
- самый активный препарат среди ФХ II поколения в отношении хламидий, микоплазм и пневмококков;
- равная с ципрофлоксацином активность против грамположительных бактерий;
- отсутствие влияния на лакто- и бифидобактерии.
2. Фармакокинетические:
- высокая биодоступность при приеме внутрь (95–100%);
- высокие концентрации в тканях и клетках, равные или превышающие сывороточные;
- низкий уровень метаболизма в печени (5–6%);
- активность не зависит от pH среды;
- выведение в неизмененном виде с мочой;
- период полувыведения 5–7 ч.
3. Клинические:
- наиболее благоприятный профиль безопасности: отсутствие серьезных нежелательных эффектов в контролируемых исследованиях;
- отсутствие клинически значимого фототоксического эффекта;
- не взаимодействует с теофиллином.
ФХ в урологической практике
Пожалуй, наиболее активно ФХ используются в урологической практике для антибактериальной профилактики и терапии ИМП. Препарат для антибактериальной терапии (АБТ) ИМП должен характеризоваться следующими свойствами:
- доказанной клинической и микробиологической эффективностью;
- высокой активностью в отношении основных уропатогенов, низким уровнем микробной резистентности в регионе;
- способностью создавать высокие концентрации в моче;
- высокой безопасностью;
- удобством приема, хорошим комплайнсом больных.
Важно выделять амбулаторные и нозокомиальные ИМП. При ИМП, возникших вне стационара, основным возбудителем является E. coli (до 86%), а другие микроорганизмы встречаются значительно реже: Klebsiella pneumoniae – 6%, Proteus spp. – 1,8%, Staphylococcus spp. – 1,6%, P. aeruginosa – 1,2%, Enterococcus spp. – 1%. При нозокомиальных ИМП лидирует также E. coli, однако значительно возрастает роль других микроорганизмов и микробных ассоциаций, намного чаще встречаются полирезистентные возбудители, а чувствительность к АБП различается между стационарами.
По данным проведенных в России многоцентровых исследований резистентность уропатогенов к широко применяемым АБП, таким как ампициллин и ко-тримоксазол, достигает 30%. Если уровень резистентности уропатогенных штаммов E. coli к антибиотику составляет в регионе более 10–20%, этот препарат не должен использоваться для эмпирической АБТ. Наибольшей активностью против E. coli среди ФХ обладают офлоксацин, ципрофлоксацин, норфлоксацин. В среднем по России выделяется 4,3% штаммов E. coli, резистентных к ФХ. Сопоставимые данные получены в США и большинстве европейских стран. В то же время, например, в Испании уровень резистентности кишечной палочки к ФХ гораздо выше – 14–22%. Регионы с более высоким уровнем устойчивости E. coli к ФХ существуют и России – это Санкт-Петербург (резистентны 13% штаммов) и Ростов-на-Дону (9,4%).
Анализируя устойчивость E. coli – основного возбудителя амбулаторных и стационарных ИМП в России, можно утверждать, что ФХ (офлоксацин, ципрофлоксацин и др.) могут служить препаратами выбора для эмпирического лечения неосложненных, а в ряде случаев и осложненных ИМП.
Применение офлоксацина для профилактики и лечения ИМП
Острый цистит
Острый цистит является наиболее частым проявлением ИМП. Частота острого цистита у женщин составляет 0,5–0,7 эпизода заболевания на 1 женщину в год, а у мужчин в возрасте 21–50 лет заболеваемость крайне низка (6–8 случаев на 10 тыс. в год). Распространенность острого цистита в России, по расчетным данным, составляет 26–36 млн. случаев в год.
При остром неосложненном цистите целесообразно назначать короткие (3–5-дневные) курсы АБТ.
Однако при хроническом рецидивирующем цистите короткие курсы терапии неприемлемы – продолжительность АБТ для полной эрадикации возбудителя должна составлять не менее 7–10 дней.
При циститах офлоксацин назначают по 100 мг 2 раза в день или по 200 мг 1 раз в день. При хроническом цистите у лиц молодого возраста, особенно при наличии сопутствующих инфекций, передающихся половым путем (в 20–40% случаев вызванных хламидиями, микоплазмами или уреаплазмами), офлоксацин является приоритетным среди других ФХ.
Острый пиелонефрит
Острый пиелонефрит является самым частым заболеванием почек во всех возрастных группах; среди больных преобладают женщины. Заболеваемость острым пиелонефритом составляет в России, по расчетным данным, 0,9–1,3 млн. случаев в год.
Лечение пиелонефрита основывается на применении эффективной АБТ при условии восстановления уродинамики и, по возможности, коррекции других осложняющих факторов (эндокринные нарушения, иммунодефицит и др.). Первоначально проводится эмпирическая АБТ, которую при необходимости изменяют после получения антибиотикограммы; АБТ должна быть длительной.
Офлоксацин может применяться для лечения пиелонефрита с учетом его накопления в паренхиме почек и высоких концентраций в моче, препарат назначают по 200 мг 2 раза в сутки в течение 10–14 дней.
Простатит
Несмотря на успехи современной урологии, лечение хронического простатита по-прежнему является неразрешенной проблемой. Этиопатогенетические представления о хроническом простатите предполагают, что инфекция и воспаление запускают каскад патологических реакций: морфологические изменения в ткани предстательной железы (ПЖ) с нарушением ее ангиоархитектоники, персистирующее иммунное воспаление, гиперсенситизацию автономной нервной системы и др. Даже после элиминации инфекционного агента перечисленные патологические процессы могут сохраняться, сопровождаясь тяжелой клинической симптоматикой. Длительная АБТ рекомендована многими исследователями как компонент комплексного лечения хронического простатита категорий II, III, IV по классификации Национального института здоровья США (NIH, 1995).
Острый простатит (категория I по NIH, 1995) в 90% случаев развивается без предшествующих урологических манипуляций, а примерно в 10% случаев становится осложнением урологических вмешательств (биопсии ПЖ, катетеризации мочевого пузыря, уродинамического исследования и др.). Основой лечения служит ступенчатая АБТ в течение 2–4 нед.
Подавляющее большинство возбудителей бактериальных простатитов относятся к грамотрицательным микробам кишечной группы (E. coli, Klebsiella spp., Proteus spp., Enterobacter spp. и др.). Этиологическими факторами могут быть также C. trachomatis, U. urealiticum, S. aureus, S. saprophyticus, Trichomonas spp., Pseudomonas spp., анаэробы и др. Препаратами выбора для лечения простатита служат ФХ, которые лучше всего проникают в ткань и секрет ПЖ и перекрывают основной спектр возбудителей простатита. Условием успешной АБТ при простатите является ее достаточная длительность – в течение как минимум 4 нед с последующим бактериологическим контролем.
Офлоксацин может с успехом применяться для лечения простатита, так как он высокоактивен против хламидий, а в отношении микоплазм и уреаплазм его эффективность сопоставима с другими ФХ и доксициклином. При хроническом простатите офлоксацин назначают внутрь по 400 мг 2 раза в сутки в течение 3–4 нед. При остром простатите проводят ступенчатую терапию: препарат вначале назначают внутривенно по 400 мг 2 раза в сутки, переходя на пероральный прием после нормализации температуры тела и клинического улучшения состояния.
Рак ПЖ и ИМП
Молекулярные и генетические исследования последних лет свидетельствуют о том, что простатит может инициировать развитие рака ПЖ. Хроническое воспаление активирует канцерогенез за счет повреждения генома клетки, стимуляции клеточной пролиферации и ангиогенеза. Активно проводятся исследования эффективности антибактериальной и противовоспалительной терапии в профилактике рака ПЖ.
Воспалительные изменения ПЖ могут приводить к повышению в крови уровня простатоспецифического антигена (ПСА). Согласно современным рекомендациям повышение уровня ПСА выше возрастных норм является показанием для биопсии ПЖ. Однако при отсутствии подозрительных на рак ПЖ изменений при пальцевом ректальном исследовании возможно применение антибактериальной и противовоспалительной терапии в течение 3–4 нед с последующим контролем уровня ПСА. В случае его нормализации биопсия ПЖ не проводится.
Доброкачественная гиперплазия ПЖ и ИМП
Доброкачественная гиперплазия ПЖ
(ДГПЖ) и симптомы инфекции нижних мочевых путей очень распространены среди мужчин. Основой медикаментозного лечения ДГПЖ являются а-блокаторы и ингибиторы 5а-редуктазы. Однако общеизвестен тот факт, что ДГПЖ почти всегда сопровождается простатитом, который зачастую вносит значительный вклад в клиническую симптоматику. Поэтому АБТ в ряде случаев целесообразна при ДГПЖ. При подтвержденном воспалительном процессе необходимо назначение АБТ на срок 3–4 нед. Препаратами выбора являются ФХ с учетом спектра их антимикробного действия и фармакокинетических особенностей.
Профилактика при урологических вмешательствах
ИМП наиболее часто становятся осложнением таких вмешательств, как трансректальная биопсия ПЖ, катетеризация мочевого пузыря, комплексное уродинамическое исследование и др. По современным стандартам антибактериальная профилактика ИМП является обязательной перед инвазивными урологическими вмешательствами. Это связано с тем, что стоимость антибактериальной профилактики и связанные с ней риски намного меньше риска возникновения и стоимости лечения ИМП. Для профилактики инфекционных осложнений при большинстве трансуретральных манипуляций, а также при трансректальной биопсии ПЖ достаточно назначения одной дозы ФХ за 2 ч до вмешательства (например, 400 мг офлоксацина).
Неразрешенной урологической проблемой является катетер-ассоциированная инфекция. Колонии микроорганизмов формируют так называемые биопленки на инородных материалах, недоступные для действия АБП и антисептиков. АБП не могут ликвидировать уже сформировавшуюся биопленку, но есть данные, что профилактическое назначение ФХ (например, офлоксацина, ципрофлоксацина или левофлоксацина) может предотвращать или замедлять ее образование.
Заключение
Фторхинолоны в течение многих лет с успехом применяются для лечения инфекций мочевых путей. Офлоксацин отвечает принципам рациональной антибактериальной терапии ИМП, его применение целесообразно для лечения и профилактики ИМП – цистита, пиелонефрита, простатита. Наличие пероральной и парентеральной лекарственной форм офлоксацина делает его применение удобным в амбулаторной практике и в стационаре.
Рекомендуемая литература
Лоран О.Б., Синякова Л.А., Косова И.В. Лечение и профилактика хронического рецидивирующего цистита у женщин // Consilium medicum. 2004. Т 6. № 7. С. 460–465.
Современные клинические рекомендации по антимикробной терапии / Под ред. Страчун-ского Л.С. Смоленск, 2004.
Падейская Е.Н., Яковлев В.П. Антимикробные препараты группы фторхинолонов в клинической практике. М., 1998.
Яковлев В.П. Место офлоксацина в амбулаторной практике: опыт 15-летнего применения // Инфекции и антимикробная терапия. 2000. Т. 2. № 5. С. 154–156.
Яковлев В.П. Фармакокинетические свойства офлоксацина // Антибиотики и химиотерапия. 1996. Т. 41. № 9. С. 24–32.
Granier N. Evaluation de la toxicite des quinolones en pediatrie // Les Quinolones en Pediatrie. Paris, 1994. P. 117–121.
Kahlmeter G. An international survey of the antimicrobial susceptibility of pathogens from uncomplicated urinary tract infections: the ECO-SENS project // J. Antimicrob. Chemother. 2003. V. 51. № 1. Р. 69–76.
Karlowsky J.A., Kelly L.J., Thornsberry C. et al. Trends in antimicrobial resistance among urinary tract infection isolates of Escherichia coli from female outpatients in the United States // Antimicrob. Agents Chemother. 2002. V. 46. № 8. Р. 2540–2545.
Kaygisiz O., Ugurlu O., Kosan M. et al. Effects of antibacterial therapy on PSA change in the presence and absence of prostatic inflammation in patients with PSA levels between 4 and 10 ng/ml // Prostate Cancer Prostatic Dis. 2006. V. 9. № 3. Р. 235–238.
Sugar L.M. Inflammation and prostate cancer // Can. J. Urol. 2006. V. 13. № 1. Р. 46–47.
Terris M. Recommendations for prophylactic antibiotic use in genitourinary surgery // Contemp. Urology 2001. № 9. P. 12–27.
Warren J.W., Abrutyn E., Hebel J.R. et al. Guidelines for antimicrobial treatment of uncomplicated acute bacterial cystitis and acute pyelonephritis in women. Infectious Diseases Society of America (IDSA) // Clin. Infect. Dis. 1999. V. 29. № 4. Р. 745–758.