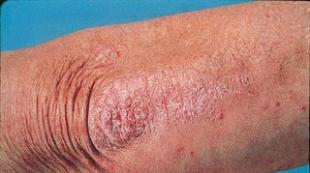
Эпидемиологические особенности формирования госпитальных штаммов в урологических отделениях. Микроорганизмы, вызывающие внутрибольничные инфекции Особенности госпитальных штаммов
Владельцы патента RU 2404254:
Изобретение относится к выявлению госпитальных штаммов микроорганизмов в лечебно-профилактических учреждениях и проведению соответствующих противоэпидемических мероприятий в них. Способ включает определение генотипических характеристик вирулентности исследуемых штаммов и сопоставление их с генотипическими характеристиками вирулентности штаммов, выделенных в лечебно-профилактическом учреждении от больных и окружающих предметов. Штаммы относят к госпитальным при соответствии генотипической характеристики вирулентности исследуемых штаммов генотипическим характеристикам вирулентности хотя бы одного из штаммов, выделенных в лечебно-профилактическом учреждении от больных и окружающих предметов. Использование способа упрощает выявление госпитальных штаммов и позволяет сократить время выявления госпитальных штаммов. 1 табл.
Изобретение относится к области медицины, а именно к эпидемиологии, и может быть использовано для выявления циркуляции госпитальных штаммов и для проведения противоэпидемических мероприятий в лечебно-профилактических учреждениях (ЛПУ).
Актуальность проблемы внутрибольничных инфекций определяется широким распространением их в медицинских учреждениях различного профиля и значительным ущербом, наносимым этими заболеваниями здоровью населения .
Для выявления циркуляции госпитальных штаммов в микробиологической практике используют методы эпидемиологического маркирования, суть которых состоит в том, что выделенные культуры идентифицируют до рода и вида, а затем проводят внутривидовую идентификацию с целью установления биовара, серовара, эковара, устойчивости к антибактериальным веществам, генотипа . Предлагаемые методы требуют значительных материальных затрат и длительного времени на проведение лабораторных исследований.
Известен способ выявления госпитальных штаммов по определению чувствительности штаммов к антибиотикам, составлению антибиотикограмм и сопоставлению антибиотикограмм культур бактерий, выделенных от больных и из окружающей среды .
Недостатком предложенного способа является недостаточная специфичность ввиду широкого распространения устойчивости к антибиотикам, в том числе у негоспитальных штаммов возбудителей, а также сложность интерпретации результатов ввиду высокой степени гетерогенности госпитальной популяции возбудителя по устойчивости к антибиотикам.
Известен способ идентификации госпитальных штаммов, включающий в себя определение биоритмов бактерий, выделенных от больных, и сравнение полученных биоритмов с биоритмами эталонных негоспитальных штаммов данного вида бактерий . Анализ биоритмов проводят по периоду репродуктивной активности бактерий, частоте ритма, мезору, амплитуде репродуктивной активности бактерий и акрофазе. При несовпадении биоритмов выделенного штамма бактерий с биоритмами эталонного негоспитального штамма выделенный штамм относят к госпитальному.
К недостаткам данного способа относится сложность интерпретации результатов, низкая специфичность ввиду значительного разнообразия госпитальных и негоспитальных генотипов, обладающих различными биоритмами. Кроме того, при осуществлении данного способа требуется круглосуточная работа врача-микробиолога, проводящего измерения через 8, 12, и 24 часа от начала исследований.
В качестве прототипа по наиболее близкой технической сущности нами выбран способ диагностики госпитального штамма синегнойной палочки PSEUDOMONAS AERUGIOSA, включающий определение чувствительности штамма к антибиотикам, его фаготипа и серотипа, устойчивости к дезинфицирующим веществам, плазмидного профиля, коэффициента адгезии к эпителиальным клеткам, штамм PSEUDOMONAS AERUGIOSA диагностируют как госпитальный при отсутствии его чувствительности к девяти и более антибиотикам, одинаковом фагосеротипе, устойчивости к пяти дезинфицирующим веществам, сходном плазмидном профиле и коэффициенте адгезии 15±0,2 и более .
К недостаткам способа, принятого за прототип, относится то, что способ является трудоемким и длительным, так как требует определения многих характеристик исследуемых штаммов, до получения окончательного результата исследования необходимо 10-15 дней. Выполнение способа требует также значительных материальных затрат.
Техническим результатом изобретения является упрощение способа выявления госпитальных штаммов и сокращение времени его проведения.
Указанный технический результат достигается тем, что определяют генотипические характеристики вирулентности исследуемых штаммов и сопоставляют их с генотипическими характеристиками вирулентности штаммов, выделенных в лечебно-профилактическом учреждении от больных и окружающих предметов. Штаммы относят к госпитальным при соответствии генотипической характеристики вирулентности исследуемых штаммов генотипическим характеристикам вирулентности хотя бы одного из штаммов, выделенных в лечебно-профилактическом учреждении от больных и окружающих предметов.
Предлагаемый способ осуществляют следующим образом.
Проводят видовую идентификацию выделенной культуры, выделяют ДНК и определяют методом полимеразно-цепной реакции или любым другим экспресс-методом наличие нуклеотидных последовательностей, соответствующих участкам генов факторов патогенности, наиболее типичных для клинически значимых изолятов данного вида.
На основании наличия тех или иных генов определяют генотипические характеристики вирулентности или патовары исследуемых штаммов и сопоставляют их с генотипическими характеристиками вирулентности или патоварами штаммов, выделенных в лечебно-профилактическом учреждении от больных и окружающих предметов и имеющих предполагаемую эпидемиологическую связь с исследуемыми штаммами. Штамм относят к госпитальным при соответствии генотипической характеристики вирулентности исследуемых штаммов генотипическим характеристикам вирулентности хотя бы одного из штаммов, выделенных от больных и окружающих предметов в лечебно-профилактическом учреждении.
Отличительными существенными признаками заявляемого способа является:
Определение генотипических характеристик вирулентности исследуемых штаммов и их сопоставление с генотипическими характеристиками вирулентности штаммов, выделенных в лечебно-профилактическом учреждении от больных и окружающих предметов;
Отнесение штамма к госпитальным при соответствии генотипической характеристики вирулентности исследуемых штаммов генотипическим характеристикам вирулентности хотя бы одного из штаммов, выделенных от больных и окружающих предметов в лечебно-профилактическом учреждении.
Причинно-следственная связь между отличительными существенными признаками и достигаемым результатом
Выбор данных генотипических характеристик в качестве основных отличительных признаков заявляемого изобретения основан на обоснованном авторами теоретическом положении о том, что именно вирулентность является основной характеристикой госпитального штамма. Так, например, отмечено возрастание уровня вирулентности в процессе формирования госпитального штамма синегнойной палочки в урологическом стационаре , Serratia marcesens в отделении реанимации новорожденных . При этом другие биологические характеристики госпитальных штаммов, такие как устойчивость к антибиотикам, являются второстепенными. Показано, в частности, что множественная устойчивость к антибактериальным препаратам может быть в равной степени свойственна как госпитальным, так и негоспитальным штаммам энтерококков . Таким образом, с нашей точки зрения, методы выявления госпитальных штаммов, основанные на определении антибиотикограмм, не являются достаточно специфичными и требуют обязательного потверждения с использованием других методов внутривидового типирования. В то же время известно, что госпитальные популяции возбудителей внутрибольничных инфекций отличаются от негоспитальных содержанием большего количества генов факторов патогенности, обуславливающих повышенную вирулентность . При этом эпидемиологически связанные культуры будут обладать одним и тем же набором факторов патогенности, представляя собой один штамм. Данное обстоятельство позволяет использовать наличие генов факторов патогенности (хотя бы одного, т.к. штаммы, не обладающие ими, не имеют клинического и эпидемического значения) и их сочетание (т.е. генотипическую характеристику вирулентности) в качестве отличительного признака госпитального штамма при условии, что другие штаммы, выделенные в лечебно-профилактическом учреждении, имеют сходную генотипическую характеристику, т.е. имеются доказательства их эпидемиологической связи.
Таким образом, использование заявляемого нами способа позволяет в кратчайшие сроки выявить основные неотъемлемые свойства госпитального штамма (вирулентность и определяющие ее генетические детерминанты) и идентифицировать на основании наличия этих свойств госпитальный штамм.
Совокупность отличительных существенных признаков является новой и позволяет, в отличие от прототипа, упростить способ выявления госпитальных штаммов и сократить время его проведения.
Примеры использования способа
В процессе эпидемиологического наблюдения в гинекологическом стационаре осуществляли определение генетических характеристик штаммов Enterococcus spp. по заявляемому способу с помощью полимеразно-цепной реакции (ПЦР) по 5 генам вирулентности - gelE, sprE, fsrB, esp u asal. Для выделения ДНК штаммы энтерококков выращивались в триптозо-соевом бульоне ("BioMerieux"), после чего ДНК выделялась методом экспресс-ПЦР.
ПЦР проводили, начиная с предварительной инкубации проб при 94°С в течение 2 мин, а затем в течение 30 циклов при следующих условиях: денатурация (94°С) - 30 сек, отжиг (47°С-65°С, в зависимости от Г-Ц состава праймеров) - 60 сек, синтез (72°С) - 60 сек, конечный синтез 10 мин при 72°С. Для амплификации были использованы праймеры, приведенные в таблице. Эксперимент выполняли на приборе MJ Research.
Результаты ПЦР оценивались после электрофореза в 1% агарозном геле в ультафиолетовом освещении.
В процессе эпидемиологического наблюдения в гинекологическом стационаре было выявлено, что у больной Л., поступившей 09.07.2005 года с диагнозом метроэндометрит (и/б №25230), на пятые сутки пребывания в отделении был выделен Е. faecium №429. На основании определения генов вирулентности данный штамм был отнесен к генотипу 2 (присутствие гена esp при отсутствии генов gelE, sprE, fsrB, asal). В тот же день этот возбудитель соответствующего генотипа был выделен из смыва с перчаток (штамм 138 вс). При эпидемиологическом обследовании выявлено, что 11.07.05 г. при осмотре больной Л. из заднего свода влагалища и цервикального канала был выделен штамм №421, сходный по генотипическим характеристикам с вышеуказанными штаммами.
В данном случае фактором передачи могли служить считающиеся стерильными перчатки, взятые для осмотра из общего бикса, который был уже вскрыт.
Таким образом, культуры №421, 429 и 138 вс имели одинаковую генотипическую характеристику, ген фактора патогенности esp и имели очевидную эпидемиологическую связь; на основании вышеперчисленных признаков они были отнесены к госпитальному штамму.
В отделении гнойной остеологии проводилось эпидемиологическое наблюдение за внутрибольничными инфекциями, обусловленными метициллин-резистентными штаммами золотистого стафилококка (MRSA). В октябре 2008 года у четырех пациентов стационара был идентифицирован MRSA с генотипом 1 (наличие гена sea, при отсутствии генов seb, sec, pvl, tst). В связи с тем, что было предположено эпидемическое распространение госпитального штамма MRSA в стационаре, было решено провести бактериологическое обследование объектов окружающей среды стационара с целью выявления факторов передачи данного штамма. В результате данного обследования было выделено 4 культуры стафилококка: 139 вс (из смыва с ручки перевязочного столика), 140 вс (из смыва с ручки крана в перевязочной), 148 вс (смыв с рук медицинской сестры А.Н.), 1а (из воздуха перевязочной). Заявляемый способ был применен для отнесения данных культур к госпитальному штамму. Определение генов вирулентности (энтеротоксины А, В, С, ген токсического шока и ген токсина Пантона-Валлентайна) проводилось по методике M.Mehrortra и Lina G
В результате проведенных исследований культуры 139 вс и 140 вс были отнесены к генотипу 1 (наличие гена sea, при отсутствии генов seb, sec, pvl, tst), культура 148 вс была отнесена к генотипу 2 (наличие генов sea, seb, при отсутствии генов sec, pvl, tst), a при исследовании культуры 1а оказалось, что она не содержит исследуемых генов факторов патогенности. Таким образом, при сопоставлении генетических характеристик исследуемых культур с генетическими характеристиками штаммов, ранее обнаруженных в стационаре, культуры 139 вс и 140 вс были отнесены к госпитальному штамму, а культуры 148 вс и 1а не были отнесены к госпитальным.
Заявляемый способ апробирован при организации эпидемиологического наблюдения за внутрибольничными инфекциями в стационарах Санкт-Петербурга (гинекологическое отделение ГУЗ "Мариинская больница", отделение гнойной остеологии больницы им. Петра Великого, стационар городского центра профилактики СПИД и инфекцонных заболеваний). Всего было исследовано 105 штаммов энтерококков, 61 штамм золотистого стафилококка. В первых двух стационарах апробация заявляемого способа позволила выявить формирование госпитальных штаммов энтерококков и золотистого стафилококка. В связи с тем, что традиционно применяемый метод отнесения культур к госпитальному штамму, основанный на определении антибиотикограммы, обладает недостаточной специфичностью, для верификации правильности отнесения исследуемых культур к госпитальному штамму был использован метод эпидемиологического маркирования . Для определения принадлежности выделяемых культур к одному штамму (клональному типу) использована комбинацию нескольких методов внутривидового типирования, являющихся независимыми по отношению друг к другу (фаготип и антибиотикограмма для энтерококков, типирование методом электрофореза ДНК в пульсирующем поле, spa-сиквенстип и антибиотикограмма для стафилококков), а для доказательства того, что данный штамм вызывал связанные случаи заболеваний в стационаре, использован метод эпидемиологического наблюдения. Использование комбинации методов внутривидового типирования в сопоставлении с эпидемиологическими данными позволяет надежно идентифицировать госпитальный штамм . Всего с использованием заявляемого способа и метода сравнения было протестировано 38 культур микроорганизмов. Во всех случаях применение указанного методического приема позволило подтвердить правильность отнесения исследуемых культур к госпитальному штамму.
Таким образом, заявляемый способ позволяет идентифицировать госпитальные штаммы.
В отличие от способа, выбранного в качестве прототипа, заявляемый способ выявления госпитальных штаммов позволяет существенно сократить затраты времени на идентификацию госпитального штамма.
По нашим наблюдениям затраты времени по выявлению 5 генов факторов патогенности в 10 бактериальных штаммах составляют от 7 до 12 часов (от момента получения чистой культуры микрорганизма), таким образом, процесс отнесения исследуемого штамма к госпитальным составляет не более двух рабочих дней, в отличие от 10-15 дней при идентификации госпитального штамма способом, выбранным в качестве прототипа.
Для выполнения данного способа, в отличие от прототипа, не требуется высокой квалификации медицинского персонала, предполагающей овладение сложными молекулярно-генетическими (выделение и рестрикция плазмид) и микробиологическими (определение адгезии микроорганизма к эпителию) методиками. Кроме того, процесс идентификации генов методом ПЦР в отличие от характеристик, определяемых по способу, выбранному в качестве прототипа, может быть частично или полностью автоматизирован при использовании робототехники, что существенно сокращает затраты времени и трудовые затраты.
К особенностям предлагаемого способа относится также легкость интерпретации результатов, поскольку отнесение исследуемой культуры к госпитальным штаммам производится на основании всего лишь одного критерия - соответствии генотипической характеристики вирулентности исследуемого штамма генотипическим характеристикам вирулентности хотя бы одного из штаммов, выделенных от больных и окружающих предметов в лечебно-профилактическом учреждении.
Таким образом, заявляемый способ позволяет упростить выявление госпитальных штаммов и сократить время проведения способа.
Литература
1. Семина Н.А. Внутрибольничные инфекции как проблема биобезопасности. /Н.А.Семина. //Вестник Российской АМН. - 2002. - №10. - С.48-50.
2. Зуева Л.П., Яфаев Р.Х. Эпидемиология: Учебник. - СПб, 2006. - 752 с.
3. Пфаллер М.А., Кормикан М.Дж. Микробиологические аспекты проблемы внутрибольничных инфекций: роль клинической лаборатории. В кн. Р.П.Венцель. Внутрибольничные инфеции. М. 2004. - 840 с.
4. RU 2245922, 10.02.2005.
5. RU 2285258, 10.10.2006.
6. RU 2110579, 10.05.1998.
7. Яфаев Р.Х., Зуева Л.П. Эпидемиология внутрибольничной инфеции. Л.: Медицина, 1989. - 168 с.
8. Любимова А.В., Зуева Л.П., Еремин С.Р., Хрусталева Н.М., Любименко В.А., Пулин A.M., Шулаева С.В., Лещинская В.Н. Успехи внедрения системы инфекционного контроля в отделениях реанимации новорожденных. В кн.: Л.П. Зуева. Опыт внедрения инфекционного контроля в лечебно-профилактических учреждениях. СПб. 2003, с.91-129.
9. Яфаев Р.Х., Колоджиева В.В., Ермоленко Е.И., Суворов А.Н. Энтерококковые инфекции урогенитального тракта в условиях стационара и поликлиники. Стационарзамещающие технологии. Амбулаторная хирургия. №3 (23), 2006 г.
10. Becker К., A.W.Friedrich, G.Lubritz, M.Weilert, G.Peters, and C. von Eiff. 2003. Prevalence of genes encoding pyrogenic toxin superantigens and exfoliative toxins among strains of Staphylococcus aureus isolated from blood and nasal specimens. J. Clin. Microbiol. 41:1434-1439.
11. Schmidt, H. and Hensel, M. (2004) Pathogenicity islands in bacterial pathogenesis. Clin. Microbiol. Rev., 17, 14-56. 12, 656-664.
12. Mehrotra M., Wang G. and Johnson W.M. Multiplex PCR for detection of genes for Staphylococcus aureus enterotoxins, exfoliative toxins, toxic shock syndrome toxin 1, and methicillin resistance.// J. Clin. Microbiol. - 2000, 38, 3: 1032-1035.
13. Lina G., Piemont Y., et al. Involvement of Panton-Valentine leukocidin-producing Staphylococcus aureus in primary skin infections and pneumonia. Clin Infect Dis 1999; 29:1128-1132.
14. Шагинян И.А. Роль и место молекулярно-генетических методов в эпидемиологическом анализе внутрибольничных инфекций. Клин. микробиология и антимикробная химиотерапия." 2000. - Т2, №3, с.82-95.
| Гены и праймеры | Последовательность нуклеотидов 5′-3′ | Ожидаемый размер продукта амплификации н.п. | |
| gelE | gelE 1 | ACCCCGTATCATTGGTTT | 419 |
| gelE 2 | ACGCATTGCTTTTCCATC | ||
| esp | esp 1 | TTGCTAATGCTAGTCCACGACC | 933 |
| esp 2 | GCGTCAACACTTGCATTGCCGAA | ||
| sprE | spr 1 | GCGTCAATCGGAAGAATCAT | 233 |
| spr 2 | CGGGGAAAAAGCTACATCAA | ||
| fsrB | fsr 1 | TTTATTGGTATGCGCCACAA | 316 |
| fsr 2 | TCATCAGACCTTGGATGACG | ||
| asal | asa 1 | CCAGCCAACTATGGCGGAATC | 529 |
| asa 2 | CCTGTCGCAAGATCGACTGTA |
Способ выявления госпитальных штаммов, включающий определение генотипа штамма, отличающийся тем, что определяют генотипические характеристики вирулентности исследуемых штаммов и сопоставляют их с генотипическими характеристиками вирулентности штаммов, выделенных в лечебно-профилактическом учреждении, от больных и окружающих предметов, штаммы относят к госпитальным при соответствии генотипической характеристики вирулентности исследуемых штаммов генотипическим характеристикам вирулентности хотя бы одного из штаммов, выделенных в лечебно-профилактическом учреждении, от больных и окружающих предметов.
Актуальность и значимость проблемы
Внутрибольничные инфекции (ВБИ, синонимы: госпитальные, нозокомиальные, больничные инфекции) представляют одну из наиболее актуальных проблем здравоохранения во всех странах мира. Наносимый ими социально-экономический ущерб огромен и трудноопределим. Парадоксально, но несмотря на колоссальные достижения в области лечебно-диагностических технологий, в частности технологий стационарного лечения, проблема ВБИ остаётся одной из наиболее острых и приобретает всё большую медицинскую и социальную значимость. Согласно данным отечественных и зарубежных исследователей, ВБИ развиваются у 5-20% госпитализированных больных.
Истоки ВБИ уходят корнями в далёкое прошлое. Инфекционные заболевания, связанные с различными медицинскими вмешательствами и манипуляциями, возникли после появления людей, занимающихся лечением, а инфекционные заболевания в стационарах - со времени формирования лечебных учреждений и принципов госпитального лечения. Сейчас можно только предположить урон, нанесённый человечеству ВБИ за это время. Достаточно вспомнить слова Н.И. Пирогова: «Если я оглянусь на кладбища, где схоронены заражённые в госпиталях, то не знаю, чему больше удивляться: стоицизму ли хирургов или доверию, которым продолжают пользоваться госпитали у правительства и общества. Можно ли ожидать истинного прогресса, пока врачи и правительство не вступят на новый путь и не примутся общими силами уничтожать источники госпитальных миазм».
В 1867 г. Джозеф Листер впервые высказал мысль о том, что раневые инфекции, широко распространённые в хирургических отделениях и приводящие к высокой смертности, вызывают живые агенты. Позднее идею экзогенного заражения Листер связал с исследованиями Л. Пастера и разработал стройную, теоретически обоснованную систему мер профилактики раневой инфекции (антисептика с элементами асептики). Он подчёркивал важность уничтожения микроорганизмов на объектах окружающей среды, соприкасающихся с раной, и защиты её от воздуха. Учение Листера заложило фундамент профилактики раневой инфекции.
В 50-60-е годы XX века остроту проблемы борьбы с ВБИ первыми ощутили экономически развитые страны, где на фоне успехов, достигнутых в борьбе со многими инфекционными и соматическими заболеваниями, отмечали рост заболеваемости ВБИ. Развитие сети стационаров и увеличение объёма больничной помощи в развивающихся странах привели к увеличению заболеваемости ВБИ, ставшими глобальной проблемой здравоохранения.
Рост ВБИ в современных условиях порождён комплексом следующих основных факторов.
Создание крупных больничных комплексов со своеобразной экологией: большой плотностью населения, представленного преимущественно ослабленными контингентами (пациентами) и медицинским персоналом. Постоянное и тесное общение больных между собой, замкнутость окружающей среды (палаты для больных, кабинеты для диагностики и лечебных процедур), своеобразие её микрофлоры, представленной преимущественно устойчивыми к антибиотикам штаммами условно-патогенных микроорганизмов.
Формирование мощного искусственного (артифициального) механизма передачи возбудителей инфекций, обусловленного инвазивными лечебными и диагностическими процедурами. Существенное значение имеет всё более широкое применение сложной техники для диагностики и лечения, требующей особых методов стерилизации.
Активация естественных механизмов передачи возбудителей инфекционных
болезней, особенно воздушно-капельного и контактно-бытового, в условиях тесного общения больных и медицинского персонала в лечебных учреждениях.
Большое количество источников инфекции в виде пациентов, поступающих в стационар с нераспознанными инфекционными болезнями, а также лиц с ВБИ, осложняющими основное заболевание в стационаре. Важная роль принадлежит медицинскому персоналу (носителям, больным стёртыми формами).
Широкое, подчас бесконтрольное применение антимикробных препаратов. Не всегда достаточно продуманная стратегия и тактика их назначения для лечения и профилактики заболеваний способствует появлению лекарственной устойчивости микроорганизмов.
Формирование госпитальных штаммов микроорганизмов, характеризующихся высокой устойчивостью к лекарственным средствам и неблагоприятным факторам окружающей среды (ультрафиолетовому облучению, высушиванию, действию дезинфицирующих препаратов).
Увеличение количества групп риска, формируемых пациентами, выхаживаемы-
ми и излечиваемыми благодаря достижениям современной медицины.
Общее снижение резистентности организма у населения в силу его эволюцион-
ной неподготовленности к стремительно изменяющимся условиям жизни в связи с бурным научно-техническим прогрессом и его теневыми сторонами - загрязнением окружающей среды, экологическим кризисом, изменением условий жизни населения (гиподинамия, стресс, неблагоприятное воздействие на организм шума, вибрации, магнитных полей и др.).
Медленная психологическая перестройка части клиницистов, по-прежнему рассматривающих многие ВБИ (пневмонию, , воспалительные заболевания кожи, подкожной клетчатки и др.) как неинфекционную патологию и несвоевременно осуществляющих или вовсе не проводящих необходимые профилактические и противоэпидемические мероприятия.
В последние годы отмечено увеличение количества лиц с различными нарушениями в системе иммунитета; для них ВБИ становятся основной причиной заболеваемости и смертности.
Присоединяющиеся ВБИ перечёркивают усилия, затраченные на проведение сложнейших операций или выхаживание новорождённых. Наслаиваясь на основное заболевание, ВБИ оказывают большое влияние на состояние организма: ведут к удлинению сроков лечения, хронизации процесса, а в наиболее тяжёлых случаях - к смерти больного.
Длительное время к ВБИ относили только заболевания, возникающие в результате заражения в больнице. Именно эта часть ВБИ, конечно, самая заметная и значительная, привлекала в первую очередь внимание общественности и медицинских работников. Сегодня, согласно определению , к ВБИ относят «любое клинически распознаваемое инфекционное заболевание, поражающее больного в результате его поступления в больницу или обращения в неё за лечебной помощью или сотрудников больницы вследствие их работы в данном учреждении, вне зависимости от появления симптомов заболевания во время пребывания в больнице или после выписки».
Из этого определения следует, что в понятие ВБИ входят как заболевания пациентов, получавших медицинскую помощь в стационарах и поликлиниках, медико-санитарных частях, здравпунктах, на дому и т.д., так и случаи инфицирования медицинского персонала в процессе их профессиональной деятельности.
Всё большее беспокойство эта проблема вызывает в России. Ежегодно, по далеко не полным данным, в Российской Федерации регистрируют 50-60 тыс. случаев ВБИ. Вместе с тем регистрируемый уровень заболеваемости ВБИ в России далеко не полностью отражает истинное положение вещей.
Проблему ВБИ изучают и рассматривают в различных аспектах, в том числе в экономическом и социальном. Экономический ущерб, вызванный ВБИ, складывается из прямых и дополнительных затрат, связанных с увеличением срока пребывания пациента в стационаре, лабораторным обследованием, лечением (, иммунопрепараты и др.). По данным американских авторов, стоимость дополнительного пребывания в стационаре из-за ВБИ составляет ежегодно от 5-10 млрд долларов США, в Венгрии - 100-180 млн форинтов, в Болгарии - 57 млн левов, в Германии - 800 тыс. марок.
Социальный аспект ущерба касается нанесения вреда здоровью пострадавшего, вплоть до инвалидности при некоторых нозологических формах, а также увеличения летальности пациентов. По данным , показатель летальности среди госпитализированных с ВБИ в 10 раз превышал таковой у лиц без инфекции.
Особенности эпидемического процесса гнойно-септической инфекции:
Перманентное течение с вовлечением в него большого количества больных и медицинского персонала;
Формирование госпитальных штаммов. В литературе широко используется термин госпитальный штамм микроба, однако единого понимания этого понятия не существует. Некоторые считают, что госпитальный штамм это тот, который выделяется от больных независимо от его свойств.
Чаще всего под госпитальными штаммами понимаются культуры, которые выделяются от больных в стационаре и характеризуются ярко выраженный резистентностью к некоторому количеству антибиотиков, т.е согласно этому пониманию, госпитальный штамм есть результат селективного действия антибиотиков. Именно такое понимание вложено в первое, имеющееся в литературе, определение госпитальных штаммов, данное В.Д. Беляковым и соавторами.
Штаммы бактерий, выделенные от пациентов с нозокоминальными инфекциями, как правило, более вирулентны и обладают множественной химиорезистентностью. Широкое использование антибиотиков с лечебной и профилактической целями лишь частично подавляет рост устойчивых бактерий и приводит к селекции устойчивых штаммов. Происходит формирование порочного круга - возникающие внутрибольничные инфекции требуют применения высокоактивных антибиотиков, способствующих в свою очередь появлению более устойчивых микроорганизмов. Не менее важным фактором следует считать развитие дизбактериозов, возникающих на фоне антибиотикотерапии и приводящих к колонизации органов и тканей условно-патагенными микроорганизмами Таб. 1. Факторы, предрасполагающие к развитию инфекций.
Внешние факторы специфичны для любого стационараМикрофлора пациентаИнвазивные медицинские манипуляции, проводимые в стационареМедицинский персоналАппаратура и инструментарийКожные покровыДлительная катетеризация вен и мочевого пузыряПостоянное носительство патогенных микроорганизмовПищевые продуктыЖКТИнтубацияВременное носительство патогенных микроорганизмовВоздухМочеполовая системаХирургические нарушение целостности анатомических барьеровБольные или инфицированные сотрудникиЛекарственное средствоДыхательные путиЭндоскопияТаб.2. Основные возбудители внутрибольничных инфекции БактерииВирусыПростейшиеГрибыСтафилококк иHBV, HCV,HDVПневмоцистыКандидаСтрептококкиHIV АспиргиллыСинегнойная палочкаВирусы гриппа и другие ОРВИКриптоспоридииЭторобактерииВирус кориЭшерихииВирус краснухиСальмонеллыВирус эпидемиоло-гичесокго паротитаШигеллыИерсинииРотавирусМистерия КамбилобактерииЭнтеробактерииЛегионеллыВ ирус герпесаКлостридииЦитомегаловирусНеспороо бразую-щие анаэробные бактерииМикоплазмыХломидииМикобактерииБо рдетеллыТаб.3. Основные источники госпитальных инфекций ИсточникРоль источника в распространенииБольныеОсновной источник роль в распространении при различных нозологических формах и в различных стационарах варьируетНосителиИмеет большое значение в распространении стафилококковых инфекций, гепатитов B, C и D, сальмонеллез, шигеллез и др. Медицинские работникиЧаще бессимптомые носители преимущественно госпитальных штаммов играют важную роль в распространении возбудителей респираторных инфекций пневмоцитозов, пневмоний, бронхитов и ОРВИ. Частота носительства могу достигать 50.Лица, привлекаемые к уходу за больнымиБольшого значения не имеют, могут быть носителями стрептококков, стафилококков, энтеро - и камбилобактерий, возбудителей венерических болезней, ротавирусов, цитомегаловирусов и прочих герпетовирусов, возбудителей гепатитов и дифтерии, пневмоцист. Посетители, навещающие больныхРоль очень ограничена, могу быть носителями стафилококков, энтеробактерий либо болеть ОРВИ. Таб.4. Передача инфекции больничному персоналу и от больничного персонала ЗаболеванияПуть передачиОт больного к медицинскому персоналуОт медицинского персонала к больномуСПИД Ветреная оспа диссемированный опоясывающий лишайВысокий ВысокийЛокализованный опоясывающий лишайНизкий НизкийВирусный коньюктивитВысокийВысокийЦитомегаловирус ная инфекцияНизкий-Гепатит АНизкийРедко Гепатит ВНизкийРедкоГепатит ни А ни ВНизкий-Простой герпесНизкийРедко ГриппУмеренныйУмеренныйКорьВысокийВысоки йМенингококковая инфекцияРедко-Эпидемиологический паротитУмеренныйУмеренныйКоклюшУмеренный УмеренныйРеспираторный синцитиальный вирусУмеренныйУмеренныйРотавирусУмеренны йУмеренныйКраснухаУмеренныйУмеренныйSalm onellaShigellaНизкийНизкийЧесоткаНизкийН изкийS. aureus-РедкоСтрептококк, группа А-РедкоСифилисНизкий-ТуберкулезОт низкого до высокогоОт низкого до высокого 3 Объекты, материалы и методы исследования Объектами исследования при проведении бактериологического контроля являются - воздушная среда - различные объекты внешней среды - хирургический инструментарий - шприцы, иглы - системы переливания крови многократного использования зонды, катетеры, бужи, резиновые перчатки и др.изделия из резины и пластикатов - хирургический шовный материал, подготовленный к использованию - руки хирургов и кожа операционного поля. Изучение санитарно-гигиенических условий включает определение температуры воздуха в основных помещениях больничные палаты, процедурные, перевязочные, операционные и другие помещения с применением ртутных и спиртовых термометров, относительную влажность измеряется с помощью психрометра Ассмана, скорость движения воздуха шаровым кататерометром, освещенность люксиметром Ю-16. Замеры проводится по общепринятым методам согласно современных нормативных документов.
В понятия микробиологический контроль стационара включается бактериологическое обследование объектов окружающей среды на наличие патогенных микроорганизмов, способных вызвать внутрибольничные инфекции.
Плановый бактериологический контроль основывается на определении общего микробного обсеменения и определения санитарно-показательных микроорганизмов стафилококки, бактерии группы кишечной палочки и др При проведении бактериологических исследований набор помещений, в которых производится отбор проб, и перечень предметов окружающей среды, подвергающихся обследованию, определяется в соответствии с приказом МЗ СССР 720 от 31.07.1978 г. 3.1
Конец работы -
Эта тема принадлежит разделу:
Санитарно-микробиологические исследования и контроль в лечебно-профилактических учреждении за внутрибольничными инфекциями
Присоединяясь к основному заболеванию, В. и. ухудшает течение и прогноз болезни. Проблемы В. и. приобрели большую актуальность в связи с появлением так.. Они легко распространяются среди детей и ослабленных, особенно пожилых, больных со сниженной иммунологической..
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ:
Что будем делать с полученным материалом:
Если этот материал оказался полезным ля Вас, Вы можете сохранить его на свою страничку в социальных сетях:
Циркулирующие в стационарах возбудители внутрибольничных инфекций постепенно формируют так называемые госпитальные штаммы , т. е. штаммы наиболее эффективно адаптированные к местным особенностям того или иного отделения.
Главной особенностью госпитальных штаммов является повышенная вирулентность (во всех случаях это первая и главная особенность госпитального штамма), а также специфическая адаптация к используемым лечебным препаратам (антибиотики, антисептики, дезинфектанты и т. п.). В настоящее время сложилась система, по которой о госпитальном штамме судят по спектру устойчивости к антибиотикам.
Условия, в которых условно-патогенные микроорганизмы способны вызвать заболевание, и особенности госпитальной среды, которые способствуют реализации этих условий
Это удобная и доступная в практических условиях система контроля формирования госпитального штамма возбудителями внутрибольничных инфекций, поскольку имеются неопровержимые данные о связи между используемыми антибиотиками в стационаре и спектром резистентности возбудителей. Но при этом надо иметь в виду, что такие штаммы оказываются чрезвычайно опасными не только из-за устойчивости к лечебным препаратам, но и в связи с их повышенной (причем иногда значительно) вирулентностью (у них меньшая инфицирующая доза, приобретены дополнительные факторы патогенности и т. д.).
Госпитальные штаммы в результате устойчивой циркуляции в лечебном учреждении приобретают дополнительные внутривидовые характеристики, позволяющие эпидемиологам устанавливать эпидемиологические связи между пациентами, определять пути и факторы передачи.
Условно-патогенные микроорганизмы вызывают основную часть внутрибольничных инфекций . В отечественной литературе для обозначения внутрибольничных инфекций, вызываемых УПМ, часто используется термин «гнойно-септические инфекции» (ГСИ), хотя этот термин иногда вызывает недоумение клиницистов (гнойное отделяемое не всегда сопровождает течение инфекции, вызванной УПМ). Причина доминирования условно-патогенных микроорганизмов в этиологической структуре ВБИ заключается в том, что именно в госпитальных условиях условно-патогенные микроорганизмы встречают те самые условия, которые обеспечивают их способность вызывать клинически выраженные заболевания.
Внутрибольничные инфекции (также госпитальные , нозокомиальные ) - согласно определению ВОЗ, любые клинически выраженные заболевания микробного происхождения, поражающие больного в результате его госпитализации или посещения лечебного учреждения с целью лечения, либо в течение 30 дней после выписки из больницы (например, раневая инфекция), а также больничный персонал в силу осуществления им деятельности, независимо от того, проявляются или не проявляются симптомы этого заболевания во время нахождения данных лиц в стационаре.
Инфекция считается внутрибольничной, если она впервые проявляется через 48 часов или более после нахождения в больнице, при условии отсутствия клинических проявлений этих инфекций в момент поступления и исключения вероятности инкубационного периода. На английском языке такие инфекции называются nosocomial infections , от др.-греч. νοσοκομείον - госпиталь (от νόσος - болезнь, κομέω - забочусь).
Госпитальные инфекции следует отличать от часто смешиваемых с ними смежных понятий ятрогенных и оппортунистических инфекций.
Ятрогенные инфекции - инфекции, вызванные диагностическими или терапевтическими процедурами.
Оппортунистические инфекции - инфекции, развивающиеся у больных с поврежденными механизмами иммунной защиты.
История
Со времени учреждения первого родильного дома в XVII веке и вплоть до середины XIX века в европейских роддомах свирепствовала родильная горячка, во время эпидемий которой смертность уносила в могилу до 27% рожениц. Справиться с родильной горячкой удалось только после того, как была установлена ее инфекционная этиология и внедрены методы асептики и антисептики в акушерстве.
Примеры внутрибольничных инфекций
- Вентилятор-ассоциированная пневмония (ВАП)
- Туберкулез
- Инфекции мочевыводящих путей
- Госпитальная пневмония
- Гастроэнтерит
- Золотистый стафилококк
- Метициллин-резистентный золотистый стафилококк (MRSA)
- Синегнойная палочка
- Acinetobacter baumannii
- Stenotrophomonas maltophilia
- Ванкомицин-резистентные энтерококки
- Clostridium difficile
Эпидемиология
В США, по оценкам Центров контроля и профилактики заболеваний, около 1,7 миллиона случаев внутрибольничных инфекций, вызванных всеми типами микроорганизмов, приводят или сопутствуют 99 000 смертям ежегодно.
В Европе, по результатам проведенных госпитальных исследований, смертность от внутрибольничных инфекций составляет 25 000 случаев в год, из них две трети вызваны грам-отрицательными микроорганизмами.
В России официально фиксируется около 30 тысяч случаев ежегодно, что свидетельствует о недостатках статистики. Исследование, проведенное в 32 скоропомощных больницах страны, показало, что госпитальные инфекции развиваются у 7,6 процентов больных, находящихся на лечении в стационаре. Если учесть, что примерное количество пролеченных в стационарах в России составляет 31-32 миллиона пациентов, то госпитальных инфекций у нас должно быть 2 миллиона 300 тысяч случаев в год.
Внутрибольничными агентами могут вызываться тяжёлые пневмонии, инфекции мочевыводящих путей, крови и других органов.
Для ВБИ характерны свои особенности эпидемиологии, отличающие её от классических инфекций. К ним относятся: своеобразие механизмов и факторов передачи, особенности течения эпидемиологического и инфекционного процессов, важная роль медицинского персонала ЛПУ в возникновении, поддержании и распространении очагов ВБИ.
Многие типы инфекций трудно поддаются лечению по причине антибиотикорезистентности, которая постепенно начинает распространяться и среди грам-отрицательных бактерий, опасных для людей во внебольничной среде.
Для возникновения ВБИ необходимо наличие следующих звеньев инфекционного процесса:
- источник инфекции (хозяин, пациент, медработник);
- возбудитель (микроорганизм);
- факторы передачи
- восприимчивый организм
Источниками в большинстве случаев служат:
- медицинский персонал;
- носители скрытых форм инфекции;
- больные с острой, стёртой или хронической формой инфекционных заболеваний, включая раневую инфекцию;
Посетители стационаров очень редко бывают источниками ВБИ.
Факторами передачи чаще всего выступают пыль, вода, продукты питания, оборудование и медицинские инструменты.
Ведущими путями заражения в условиях ЛПО являются контактно-бытовой, воздушно-капельный и воздушно-пылевой. Также возможен парентеральный путь (характерно для гепатитов B, С, D и др.)
Механизмы передачи инфекции : аэрозольный, фекально-оральный, контактный, гемоконтактный.
Способствующие факторы
К факторам внутрибольничной среды, способствующим распространению ВБИ относятся:
- недооценка эпидемической опасности внутрибольничных источников инфекции и риска заражения при контакте с пациентом;
- перегрузка ЛПО;
- наличие невыявленных носителей внутрибольничных штаммов среди медперсонала и пациентов;
- нарушение медперсоналом правил асептики и антисептики, личной гигиены;
- несвоевременное проведение текущей и заключительной дезинфекции, нарушение режима уборки;
- недостаточное оснащение ЛПО дезинфекционными средствами;
- нарушение режима дезинфекции и стерилизации медицинских инструментов, аппаратов, приборов и т. д.;
- устаревшее оборудование;
- неудовлетворительное состояние пищеблоков, водоснабжения;
- отсутствие фильтрационной вентиляции.
Группа риска
Лица с повышенным риском заражения ВБИ:
- Больные:
- без определенного места жительства, мигрирующее население,
- с длительными недолеченными хроническими соматическими и инфекционными заболеваниями,
- не имеющие возможность получать специальную медицинскую помощь;
- Лица, которым:
- назначена терапия, подавляющая иммунную систему (облучение, иммунодепрессанты);
- проводятся обширные хирургические вмешательства с последующей кровезаместительной терапией, программный гемодиализ, инфузионная терапия;
- Роженицы и новорождённые, особенно недоношенные и переношенные;
- Дети с врождёнными аномалиями развития, родовой травмой;
- Медперсонал ЛПО.
Этиология
Всего насчитывается более 200 агентов, которые могут быть причиной ВБИ. До появления антибиотиков основными из них были стрептококки и анаэробные палочки. Однако после начала клинического применения антибиотиков возбудителями основных ВБИ стали ранее непатогенные (или условно-патогенные) микроорганизмы: St. aureus, St. epidermidis, St. saprophiticus, Escherichia coli, Enterococcus faecalis, Enterococcus durans, Klebsiella sp., Proteus mirabilis, Providencia spp, Acinetobacter, Citrobacter, Serratia marcescens .
Так же установлено, что внутрибольничное инфицирование может быть связано с распространением ротавирусной, цитомегаловирусной инфекции, кампилобактера, вирусов гепатита B, С и D, а также ВИЧ-инфекции.
В результате циркуляции микроорганизмов в отделении происходит их естественный отбор и мутация с образованием наиболее устойчивого госпитального штамма, являющегося непосредственной причиной ВБИ.
Госпитальный штамм - это микроорганизм, изменившийся в результате циркуляции в отделении по своим генетическим свойствам, в результате мутаций или переноса генов (плазмид) обретший некоторые несвойственные «дикому» штамму характерные черты, позволяющие ему выживать в условиях стационара.
Основные черты приспособления - это устойчивость к одному или нескольким антибиотикам широкого спектра действия, устойчивость в условиях внешней среды, снижение чувствительности к антисептикам.. Госпитальные штаммы очень разнообразны, в каждой больнице или отделении возможно появление своего характерного штамма со свойственным только ему набором биологических свойств.
Классификация
- В зависимости от путей и факторов передачи ВБИ классифицируют:
- Воздушно-капельные (аэрозольные)
- Вводно-алиментарные
- Контактно-бытовые
- Контактно-инструментальные
- Постинъекционные
- Постоперационные
- Послеродовые
- Посттрансфузионные
- Постэндоскопические
- Посттрансплантационные
- Постдиализные
- Постгемосорбционные
- Посттравматические инфекции
- Другие формы.
- От характера и длительности течения:
- Острые
- Подострые
- Хронические.
- По степени тяжести:
- Тяжелые
- Средне-тяжелые
- Легкие формы клинического течения.
- В зависимости от степени распространения инфекции:
- Генерализованные инфекции: бактериемия (виремия, микемия), септицемия, септикопиемия, токсико-септическая инфекция (бактериальный шок и др.).
- Локализованные инфекции
- Инфекции кожи и подкожной клетчатки (ожоговых, операционных, травматический ран, Постинъекционные абсцессы, омфалит,рожа, пиодермия, абсцесс и флегмона подкожной клетчатки, парапроктит, мастит, дерматомикозы и др.);
- Респираторные инфекции (бронхит, пневмония, легочный абсцесс и гангрена, плеврит, эмпиема и др.);
- Инфекции глаза (конъюнктивит, кератит, блефарит и др.);
- ЛОР-инфекции (отиты, синуситы, ринит, мастоидит, ангина, ларингит, фарингит, эпиглоттит и др.);
- Стоматологические инфекции (стоматит, абсцесс, др.);
- Инфекции пищеварительной системы (гастроэнтероколит, энтерит, колит, холецистит, гепатиты, перитонит, абсцессы брюшины и др.);
- Урологические инфекции (бактериурия, пиелонефрит, цистит, уретрит, др.);
- Инфекции половой системы (сальпингоофорит, эндометрит, др.);
- Инфекции костей и суставов (остеомиелит, инфекция сустава или суставной сумки, инфекция межпозвоночных дисков);
- Инфекции ЦНС (менингит, абсцесс мозга, вентрикулит и др.);
- Инфекции сердечно-сосудистой системы (инфекции артерий и вен, эндокардит, миокардит, перикардит, постоперационный медиастинит).
Профилактика
Профилактика внутрибольничных инфекций является сложным и комплексным процессом, который должен включать три составляющие:
- минимизация возможности заноса инфекции извне;
- исключение распространения инфекции между больными внутри учреждения;
- исключение выноса инфекции за пределы ЛПУ.
Лечение
Лечение внутрибольничной инфекции
В идеале следует назначить антимикробный препарат узкого спектра активности, который действует на конкретный микроорганизм, выделенный при микробиологическом исследовании. Однако, на практике внутрибольничная инфекция, особенно в первые дни, практически всегда лечится эмпирически. Выбор оптимальной схемы антимикробной терапии зависит от преобладающей микрофлоры в отделении и спектра её антибиотикорезистентности.
С целью снижения антибиотикорезистентности возбудителей следует практиковать регулярную ротацию антибактериальных препаратов (когда определённые антибиотики, используются в отделении для эмпирической терапии в течение нескольких месяцев, а затем заменяются следующей группой).
Стартовая антимикробная терапия
Внутрибольничная инфекция, вызванная грамположительными микроорганизмами, наиболее эффективно лечится ванкомицином, а отношении грамотрицательных бактерий наибольшей активностью обладают карбапенемы (имипенем и меропенем), цефалоспорины IV поколения (цефепим, цефпиром) и современные аминогликозиды (амикацин).
Из сказанного не следует делать вывод о том, что внутрибольничная инфекция поддаётся только вышеперечисленным средствам. Например, возбудители инфекций мочевыводящих путей сохраняют высокую чувствительность к фторхинолонам, цефалоспоринам III поколения и др.
Но серьёзная внутрибольничная инфекция, действительно, требует назначения карбапенемов или цефалоспоринов IV поколения, так как они обладают наиболее широким спектром активности и действуют на полимикробную флору, в том числе на полирезистентных грамотрицательных возбудителей и многих грамположительных микроорганизмов. Недостатком препаратов обеих групп является отсутствие активности в отношении метициллинрезистентных стафилококков, поэтому в тяжёлых случаях их приходится комбинировать с ванкомицином.
Кроме того, все указанные средства не действуют на грибковые патогенны, роль которых в развитии внутрибольничных инфекций существенно возросла. Соответственно, при наличии факторов риска (например, выраженный иммунодефицит) следует назначать противогрибковые средства (флуконазол и др.)
В 90-е годы ХХ века было показано, что эффективность стартовой антибактериальной терапии оказывает непосредственной влияние на летальность госпитализированных больных. Летальность среди больных, получавших неэффективную стартовую терапию, была выше, чем у пациентов, которым назначали антибиотики, активные в отношении большинства возбудителей. Более того, в случае неадекватной стартовой терапии даже последующая смена антибиотика уже с учётом микробиологических данных не приводила к снижению летальности.
Таким образом, при тяжёлых внутрибольничных инфекциях само понятие «резервный антибиотик» утрачивает свой смысл. Эффективность стартовой терапии - это важный фактор, от которого зависит прогноз для жизни.
На основании этих данных была разработана концепция деэскалационной терапии . Суть её заключается в том, что в качестве стартовой эмпирической терапии, которую начинают сразу после установления диагноза, используют комбинацию антимикробных средств, действующих на всех возможных возбудителей инфекции. Например, карбапенем или цефепим сочетают с ванкомицином (плюс флуконазол) в зависимости от состава вероятных возбудителей.
Доводом в пользу комбинированной терапии служат:
- более широкий спектр активности;
- преодоление устойчивости, вероятность которой выше при применении одного препарата;
- наличие теоретических данных о синергизме определённых средств.
До начала применения антибиотиков необходимо провести забор образцов биологических жидкостей для микробиологического исследования. После получения результатов микробиологического исследования и клинической оценки эффективности лечения через 48-72 ч возможна коррекция терапии, например, отмена ванкомицина, если выявлен грамотрицательный возбудитель. Теоретически возможна смена всей комбинации на препарат более узкого спектра действия, хотя у тяжёлого больного, ответившего на терапию, любой врач предпочтёт оставить назначенные антибиотики.
Возможность внедрения деэскалационной терапии зависит от эффективной работы микробиологической службы и степени доверия к её результатам. Если возбудитель остаётся неизвестным, то эта концепция теряет смысл и может привести к ухудшению результатов лечения. Целесообразность деэскалационной терапии следует в первую очередь обсуждать у больных с серьёзными инфекциями, угрожающими жизни (например, вентилятор-ассоциированная пневмония, сепсис).
Следует учитывать, что обратный подход (то есть эскалация терапии) в подобных ситуациях может закончиться смертью больного ещё до получения результатом микробиологического исследования.